کلر زنی رادیکال آزاد: گزینش پذیری
این پست همه چیز در مورد گزینش پذیری هالوژناسیون رادیکال آزاد: به هر حال “انتخابی بودن” به چه معناست؟ و چگونه آن را محاسبه کنیم؟ اغلب گفته می شود که کلر زنی کمتر از برم سازی “انتخابی” است. چه می کند که منظور داشتن؟ (اطلاعات بیشتر در مورد این موضوع در پست بعدی).
1. کلرزنی پروپان منجر به ترکیب “آماری” 1-کلروپروپان و 2-کلروپروپان نمی شود. چرا که نه؟
در آخرین پست چند نمونه از چگونگی تشکیل ایزومرهای مختلف در هالوژناسیون رادیکال آزاد آلکان ها را نشان دادیم. و من با یک سوال متوقف شدم.
اگر کلر زنی رادیکال آزاد را روی پروپان با 1 equiv کلر انجام دهیم2 در شرایط عادی (25 درجه سانتیگراد، شروع با نور)، نسبت مورد انتظار 1-کلروپروپان و 2-کلروپروپان چقدر است؟
توجه داشته باشید که شش هیدروژن اولیه (“متیل”) (حذف هر یک از آنها منجر به 1-کلروپروپان می شود) و دو هیدروژن ثانویه (“متیلن”) وجود دارد. این نسبت 3:1 است. اگر هالوژناسیون از نظر آماری تصادفی بود، بنابراین نسبت 75:25 1-کلروپروپان به 2-کلروپروپان را انتظار داریم.
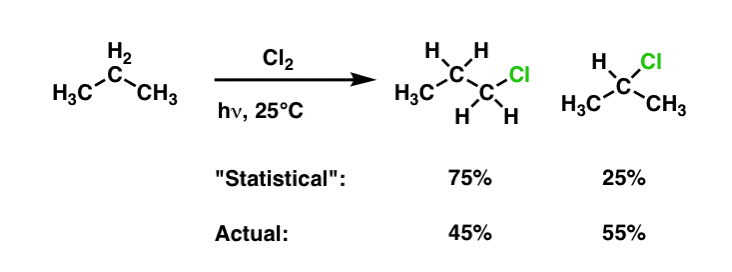
این چیزی نیست که اتفاق می افتد!
در عوض، آزمایش به ما می گوید که نسبت 55:45 2-کلروپروپان به 1-کلروپروپان را بدست می آوریم. بنابراین واضح است که این توزیع محصول بیشتر از تصادفی بودن محض است.
چرا ممکن است این باشد؟
بحث قبلی ما در مورد ثبات رادیکال های آزاد را به یاد بیاورید. مشاهده کردیم که رادیکالهای آزاد با افزایش تعداد جایگزینهای کربن، از متیل (پایدارترین) < اولیه < ثانویه < سوم (پایدارترین) پایداری را افزایش میدهند.
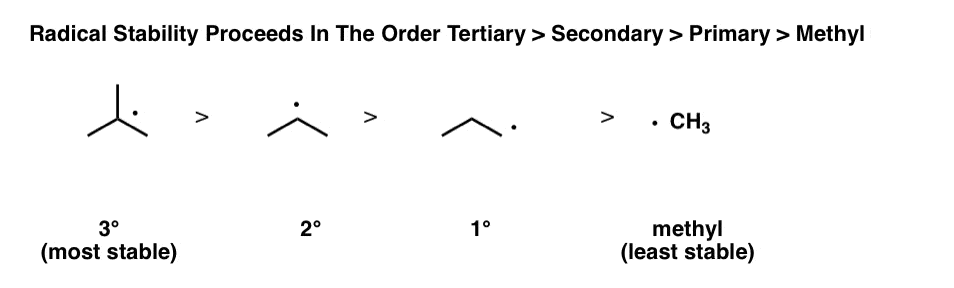
همانطور که قبلاً نیز اشاره کردیم، این نیز نسبت استحکام باند C-H است: CH4 > R–CH3 > R–CH2–R > R3C–H. هر چه رادیکال آزاد باقی مانده پایدارتر باشد، استحکام پیوند C-H ضعیف تر خواهد بود.
2. پیوندهای C-H ثانویه ضعیف تر از پیوندهای C-H اولیه هستند. شکستن پیوند C-H ثانویه منجر به رادیکال آزاد پایدارتر می شود
بیایید به پروپان بپردازیم.
در واکنش کلرزنی رادیکال آزاد، رادیکال کلر ممکن است یک هیدروژن را از یکی از گروه های متیل پروپان یا از متیلن استخراج کند.
اگر همه چیز برابر باشد، کدام یک از اینها باید ساده ترین فرآیند باشد؟

حذف هیدروژن ثانویه، به ما یک رادیکال آزاد ثانویه می دهد!
به همین دلیل است که پیوندهای C-H به طور تصادفی شکسته نمی شوند (و از این رو نسبت 75:25 را دریافت نمی کنیم). ثبات رادیکال آزاد که ما ایجاد می کنیم یک عامل بسیار مهم است.
3. نحوه تعیین کمیت “انتخاب” در کلرزنی رادیکال آزاد
این انحراف از یک مخلوط آماری به عنوان نامیده می شود گزینش پذیری. اینجا می گوییم که کلرزنی بیشتر است انتخابی برای کربن ثانویه نسبت به کربن اولیه.
بنابراین چگونه انتخاب را کمی کنیم؟
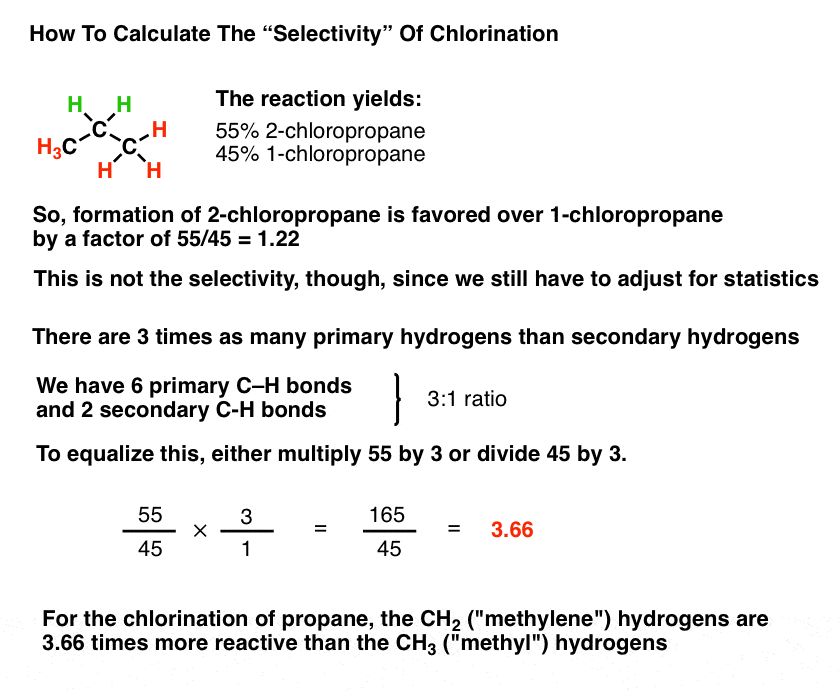
اگر تعداد مساوی متیلن وجود داشت (CH2) هیدروژن و متیل (CH3) هیدروژن ها، ساده است: 55:45 در این مورد، یا 1.22 به نفع متیلن.
با این حال، این است به همین سادگی نیست ما باید تعصب آماری را به نفع گروههای متیل تنظیم کنیم.
به یاد بیاورید که وجود دارد سه برابر متیل هیدروژن ها نسبت به متیلن هیدروژن ها. برای اینکه این نسبت واقعی باشد، باید عددی را که برای متیل به دست آوردیم بر 3 تقسیم کنیم. این نسبت 55:15 یا 3.66 را به ما می دهد.
بنابراین برای این واکنش، کلرزنی رادیکال آزاد پروپان در دمای 25 درجه سانتی گراد، کلر برای هیدروژن های ثانویه 3.66 برابر بیشتر از هیدروژن های اولیه انتخابی است.
اگر ما در حال بررسی یک واکنش بودیم که کجا سه انواع مختلفی از هیدروژن ها وجود داشت (یا حتی بیشتر) ما به همین ترتیب هر بازده را با یک عامل برابر با تعداد هیدروژن های هر نوع تنظیم می کنیم و سپس مستقیماً با هم مقایسه می کنیم.
4. یک معما: انتخاب پذیری 2-بروموپروپان در این واکنش چیست؟
بیایید با یک پازل دیگر کنار بیاییم. دقیقاً به همان واکنش نگاه کنید، به جز استفاده از Br2 به جای Cl2 . در اینجا، ما نسبت 97٪ 2-بروموپروپان به 1-bromopropane را مشاهده می کنیم.
گزینش پذیری 2-بروموپروپان در این واکنش چقدر است؟
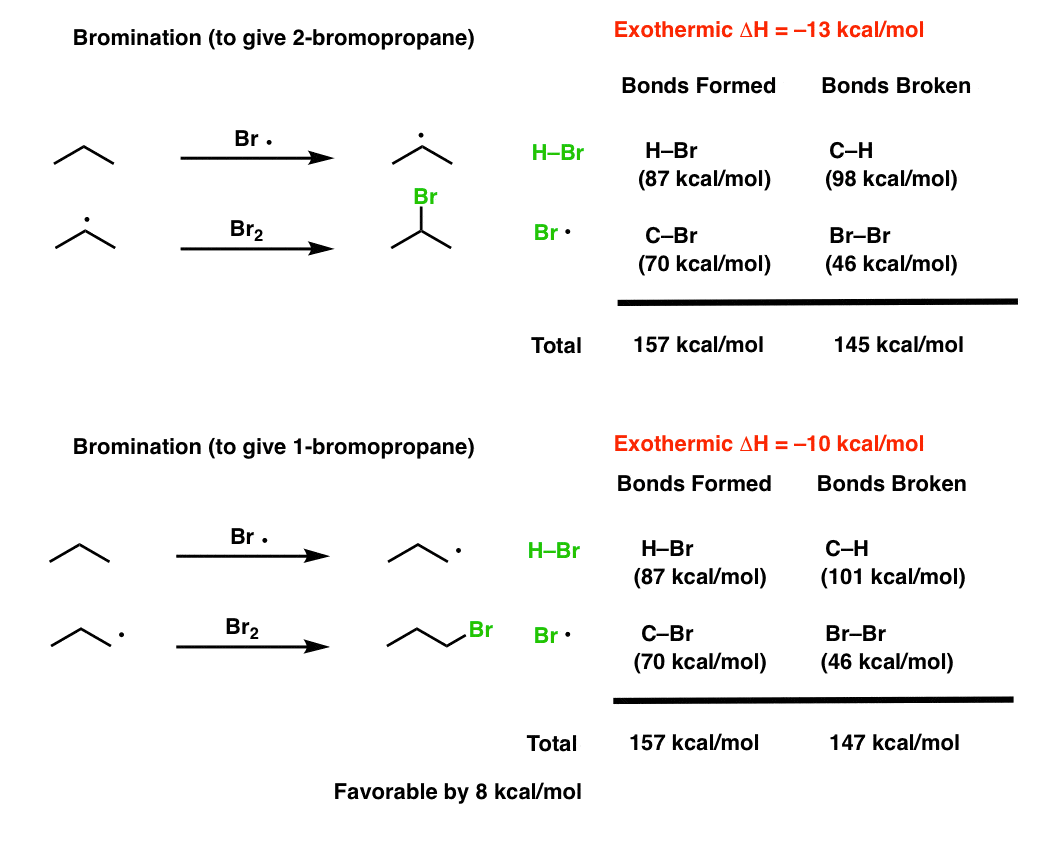
و چرا انتخاب برم ممکن است بسیار بیشتر از کلر باشد؟
دفعه بعد جواب بده!
پست بعدی: گزینش پذیری در واکنش های رادیکال آزاد – برم در مقابل کلر
(پیشرفته) مراجع و مطالعه بیشتر
- غیرمعمول و غیرمنتظره در یک واکنش قدیمی. فتوکلره آلکان ها با کلر مولکولی در محلول
KU Ingold، J. Lusztyk، و KD Raner
حساب های تحقیقات شیمیایی 1990، 23 (7)، 219-225
DOI: 10.1021/ar00175a003
این حساب اطلاعات مفید زیادی در مورد گزینش پذیری واکنش رادیکال های کلر با بسترهای آلی دارد. KU Ingold پسر شیمیدان برجسته پروفسور CK Ingold بود. - سنتز از هیدروکربن های گاز طبیعی شناسایی تک کلریدها از کلرزنی پارافین های ساده تر
HB Hass، ET McBee، و Paul Weber
شیمی صنعتی و مهندسی 1935، 27 (10)، 1190-1195
DOI: 10.1021/ie50310a025
یکی از قدیمی ترین مقالات در مورد کلرزنی هیدروکربن ها با رادیکال آزاد. جالب توجه است که نویسندگان بیان می کنند:بازآرایی اسکلت کربن در طول کلرزنی فتوشیمیایی یا حرارتی در صورت اجتناب از دمای پیرولیز رخ نمی دهد. هر مشتق تک کلریدی ممکن بدون چنین بازآرایی همیشه تشکیل می شود“. - فتوکلره 2-Methylpropane-2-d و α-d1-Toluene. مسئله بازآرایی یا تبادل رادیکال آزاد در واکنش های جانشینی
هربرت سی براون و گلن راسل
مجله انجمن شیمی آمریکا 1952، 74 (16)، 3995-3998
DOI: 1021/ja01136a007
این مقاله توسط HC براون برنده جایزه نوبل، واکنشپذیری یک اتم H در برابر یک اتم D را در یک موقعیت مشابه در کلرزنی رادیکالهای آزاد اندازهگیری میکند. همانطور که او می گوید:با مقایسه واکنش نسبی اتم های دوتریوم و هیدروژن 2-متیل پروپان-2-d (1.00:2.5) و اتم های هیدروژن سوم و اولیه ایزوبوتان (1.0:4.5)، یک دوتریوم سوم و اتم هیدروژن سوم ایزوبوتان دارای واکنش نسبی 1.0: 1.8 اندازه گیری شده در واکنش فتوکلرینه در 15-درجه“. - فتوکلره فاز مایع و کلرزنی سولفوریل کلرید هیدروکربن های شاخه دار. تأثیر ساختار بر واکنشپذیری نسبی هیدروژن سوم در کلرزنیهای رادیکال آزاد
گلن ای. راسل و هربرت سی براون
مجله انجمن شیمی آمریکا 1955، 77 (15)، 4031-4035
DOI: 1021/ja01620a021
سولفوریل کلرید (SO2Cl2) همچنین می تواند به عنوان یک عامل کلر زنی استفاده شود و با رادیکال های آلکیل در یک واکنش زنجیره ای واکنش می دهد. SO2رادیکال کلر نسبت به رادیکال کلر واکنش پذیری کمتری دارد و بنابراین انتخابی تر است. - هالوژناسیون رقابتی سیکلوهگزان و هیدروکربن های آرالکیل. شواهدی در مورد ماهیت حالات در حال گذار در واکنش های هالوژناسیون
گلن ای. راسل و هربرت سی براون
مجله انجمن شیمی آمریکا 1955، 77 (17)، 4578-4582
DOI: 1021/ja01622a041
در مقدمه آمده است: «تولوئن 60 برابر سیکلوهگزان نسبت به اتمهای برم واکنشپذیر است، در حالی که نسبت به اتمهای کلر، سیکلوهگزان 11 برابر تولوئن واکنشپذیر است». پروفسور براون این را با استفاده از اصل هاموند توضیح می دهد – برماسیون تولوئن شامل یک حالت گذار دیررس (نزدیک به رادیکال بنزیل) و کلرزنی تولوئن یک حالت انتقال اولیه است، جایی که پیوند CH هنوز عمدتاً دست نخورده است. - انتقال الکترون در حمله اتم ها یا رادیکال ها به پیوندهای کربن-هیدروژن
جی جی راسل
چهار وجهی 1959، 5 (1)، 101-104
DOI: 10.1016/0040-4020(59)80081-8
این مقاله استدلال مشابهی را برای ارجاع می دهد. #5. رادیکالهای واکنشپذیرتر (یعنی آنهایی که میل الکترونی بالاتری دارند) غنیترین اتم هیدروژن از الکترون را در مولکول انتزاع میکنند و حالت گذار با «انتقال الکترون» تثبیت میشود. رادیکالهای واکنشپذیر کمتر، انتخابیتر هستند و حالت گذار بیشتر شبیه رادیکال واسط خواهد بود، بنابراین پایداری رادیکال حاصل مسیر واکنش را دیکته میکند. - رادیکال های بسیار انتخابی کلرووینیلاسیون هگزان
فردریک اف راست و چارلز اس بل
مجله انجمن شیمی آمریکا 1970، 92 (18)، 5530-5531
DOI: 1021/ja00721a048
nهگزان با تری کلرواتیلن در یک واکنش زنجیره ای رادیکال با گزینش پذیری بالا واکنش می دهد – بیش از 80 درصد واکنش در موقعیت 2 است. - کلرزنی 2،3-دی متیل بوتان: یک آزمایش شیمی آلی کمی
هاج مارکگراف
مجله آموزش شیمی 1969، 46 (9)، 610
DOI: 10.1021/ed046p610
این مقاله یک آزمایش مناسب برای بخشهای آزمایشگاهی شیمی آلی در مقطع کارشناسی را توصیف میکند. رادیکال های کلر را می توان از SO تولید کرد2Cl2 یا NCS (N-chlorosuccinimide) و تجزیه و تحلیل توزیع محصول از واکنش با 2،3-dimethylbutane، که دارای انواع مختلفی از اتمهای هیدروژن است، انتخابپذیری را برای مکانهای سوم نسبت به اولیه نشان میدهد.
