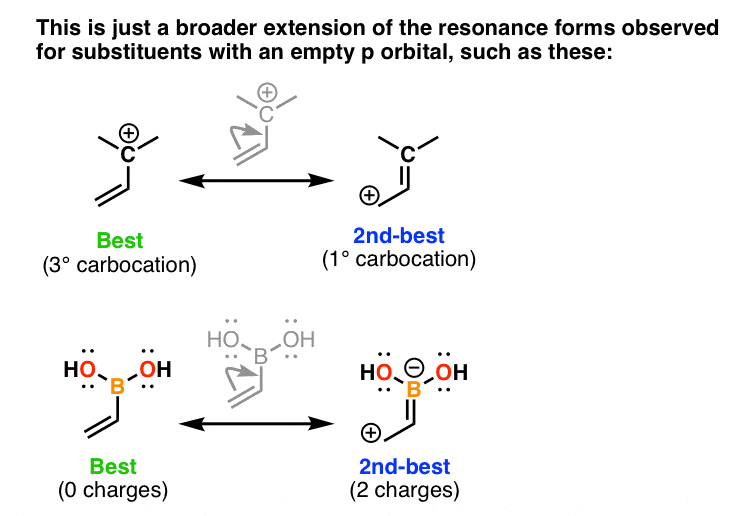
رزونانس در شیمی آلی: “پذیرنده های Pi” چیست؟
آخرین بار دیدیم که اهداکنندگان π اتم هایی هستند که قادر به تشکیل یک پیوند π جدید با پیوند CC π مجاور هستند. نتیجه اهدای π این است که این مولکولها شکل تشدید مهمی خواهند داشت که در آن کربن در انتهای پیوند π (دور از دهنده π) دارای بار منفی است.
موضوع امروز پذیرندگان π است که همانطور که تصور می کنید دقیقاً پدیده ای متضاد با اهدای π است.
1. پیوندهای پی که به سمت یک اتم الکترونگاتیو بیشتر قطبی شده اند، شکل تشدید مهمی دارند که در آن اتم الکترونگاتیو کمتر بار مثبت دارد.
به یاد بیاورید که در پیوندهای π که به سمت یک اتم الکترونگاتیو تر قطبی شده اند، یک شکل تشدید مهم داریم که در آن اتم الکترونگاتیو کمتر (معمولاً کربن) بار مثبت را تحمل می کند. این یکی در سمت چپ، پایین خواهد بود.
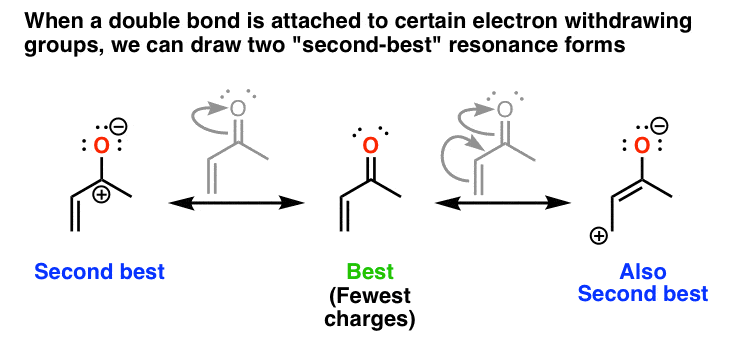
با این حال، هنگامی که ما یک پیوند دوگانه اضافی متصل به یک گروه خارج کننده الکترون داریم، می توانیم یک را نیز رسم کنیم اضافی فرم تشدید که در آن بار مثبت وجود دارد دور کربن. این یکی سمت راست خواهد بود.
این هر دو اشکال رزونانس مهمی هستند. توجه داشته باشید که هر دو دارای تعداد بار مساوی هستند (دو بار) و قطبی شده اند تا بار منفی را روی الکترونگاتیوترین اتم (اکسیژن) قرار دهند. آنها هر کدام سهم مهمی در هیبرید رزونانس این مولکول خواهند داشت.
(مسئله اینکه کدام فرم رزونانس است بیشتر برای اهداف واکنشپذیری مهم است، سؤال مهمی است که من آن را به تاریخ بعدی موکول میکنم. پاسخ کوتاه این است که تا حد زیادی به شرایط واکنش انتخاب شده بستگی دارد).
2. این گروهها را «پذیرندههای Pi» مینامند زیرا میتوانند پیوند Pi را در کنار آن «بپذیرند».
اکنون: ببینید پیوند دوگانه چگونه به سمت گروه الکترون خارج کننده “حرکت” کرده است؟ به همین دلیل، ما این نوع جانشین ها را «پذیرنده pi» می نامیم، زیرا آنها می توانند پیوند pi را «پذیرش» کنند.
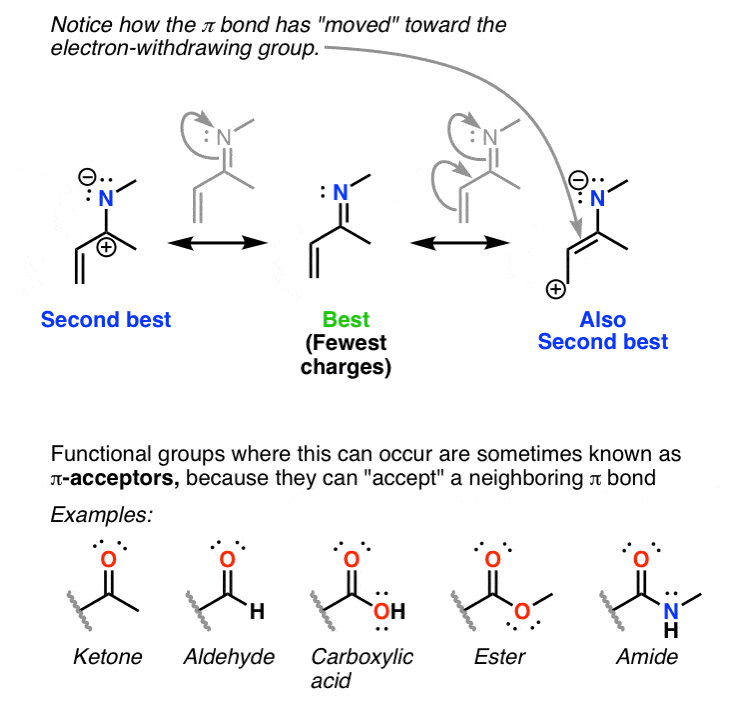
این یک پدیده عمومی است نه فقط برای گروه های عاملی حاوی گروه های C=O و C=N، بلکه برای گروه های عاملی مانند نیتریل ها، گروه های نیترو، سولفونیل ها… اساساً هر قطبی شده گروه حاوی پیوند π.
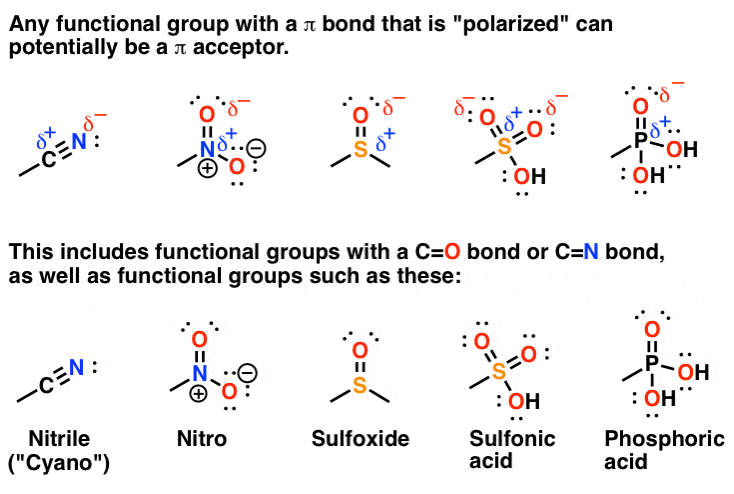
3. وجود یک “پذیرنده Pi” متصل به یک باند CC Pi منجر به شکل تشدید مهمی می شود که در آن کربن ترمینال در Pi Bond دارای بار مثبت است.
در اینجا خلاصه ای سریع از این پدیده آمده است:
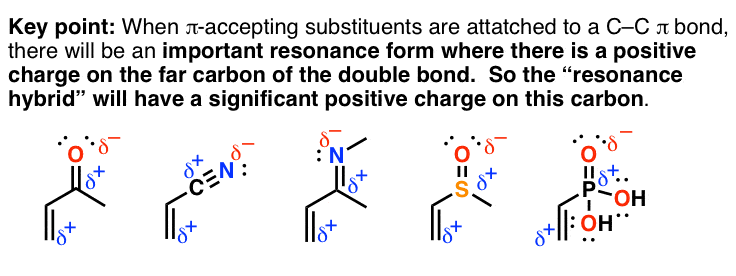
میتوانید این را بهعنوان بسط پدیدهای در نظر بگیرید که ما برای اشکال رزونانسی مشاهده میکنیم که دارای اوربیتال p خالی هستند، مانند کربوکاتیونها و سایر گروههایی که حاوی یک اوربیتال خالی p هستند (مانند این اسید بورونیک، در تصویر).
این آخرین پست بزرگی است که برای معرفی مفاهیم رزونانس در حال حاضر برنامه ریزی شده است. پس از یک خلاصه، و سپس چند نمونه از کارهایی که نباید انجام داد، من می خواهم نشان دهم که چگونه می توانید درخواست دادن این مهارت (ارزیابی اشکال رزونانس در تعیین چگالی الکترون روی یک مولکول) به سمت کشف کردن واکنش پذیری یک مولکول معین
پست بعدی: به طور خلاصه – طنین