امروز را صرف بررسی مکانیسم برخی از واکنشها در برگه خلاصهای که دفعه قبل ارسال کردم، میکنم. همانطور که در آن پست گفتم، من فکر می کنم که حدود 98٪ از مکانیسم های 110 ترکیب روی صفحه را می توان به اندازه کافی با پنج واکنش فردی توضیح داد: پروتوناسیون/پروتوناسیون، 1،2-افزودن، 1-2-حذف، 1- 4 علاوه بر این، و SN2 [It goes to 100% if you include the E2].
من فکر می کنم بهتر است با تقسیم هسته دوست ها به دو کلاس مختلف، بحث در مورد مسیرهای مکانیکی واکنش ها را در این جدول شروع کنیم: آنیونی نوکلئوفیل ها (گریناردها، انولات ها، سیانیدها، آلکوکسیدها، هیدروکسیدها و هیدریدها) و خنثی نوکلئوفیل ها (آمین ها، آمین ها، الکل ها و آب). در حالی که همه واکنشهای جدول هنوز از قانون اساسی «هوکلوفیل به الکتروفیل حمله میکند» پیروی میکنند، اما نکات ظریفی بین این دسته از هستهدوستها در مورد زمانبندی مراحل پروتونهسازی وجود دارد. علاوه بر این، واکنش های برخی از هسته دوست های خنثی را می توان با استفاده از کاتالیز اسیدی تسهیل کرد، در حالی که اسید فقط تعدادی از نوکلئوفیل های آنیونی را از بین می برد (به عنوان مثال، گریگناردز). بنابراین من این پست اول را به صحبت در مورد مکانیسم های آن اختصاص می دهم آنیونی نوکلئوفیل ها
توجه: در حالی که مکانیسم ها مهم هستند، من فکر می کنم به راحتی می توان بیش از حد در آنها پیچیده شد. من می گویم ابتدا اصول را یاد بگیرید. پوند در ازای پوند، دانستن روندها و اصول حاکم بر شیمی اساسی، شما را بهتر از دانش پیچیده مکانیزم امتحان می کند. این به این دلیل است که آزمونهای چند گزینهای و آزمونهای کوتاه پاسخ، روش ترجیحی ارزشیابی برای اکثر مربیان است: آنها امکان ارزیابی مؤثر درک شما از مفاهیم شیمیایی را فراهم میکنند، در حالی که برای نمرهدهی زمان زیادی نمیگیرند. من باید مدتی در مورد تدارکات درجهبندی پستی بنویسم: بگذارید فقط بگوییم که زمان و کار لازم برای درجهبندی سوالاتی که شامل پاسخهای کتبی طولانی است (مثلاً مکانیسمها) میتواند گسترده باشد، بهویژه برای کلاسهای بیش از ۱۰۰ دانشآموز. من نمی گویم مکانیسم ها را یاد نگیرید. من می گویم: قبل از اینکه در مورد جزئیات مثلاً یک مرحله انتقال پروتون میانی در مکانیسم آلدول گرفتار شوید، ابتدا مطمئن شوید که اصول اولیه (یعنی pKas، واکنش نسبی گروه های کربونیل) را پایین آورده اید. واکنش.
خوب. با این وجود، برای واکنش های هسته دوست های آنیونی، واقعاً فقط 5 الگوی مختلف وجود دارد.
مورد 1: 1،2-افزودن به دنبال پروتوناسیون (فرو نشاندن).
مورد 2: 1،2-افزودن به دنبال 1،2-حذف.
مورد 3: 1،4-افزودن به دنبال پروتوناسیون [check out row E]
مورد 4: SN2. (بله، همین)
مورد 5: به دلیل نبود عبارت بهتر، شکست واکنش. سه دلیل اصلی برای این امر وجود دارد: 1) پروتوناسیون برگشت ناپذیر نوکلئوفیل توسط الکتروفیل (مثلا گریگنارد با اسیدهای کربوکسیلیک) 2) تلاش برای جابجایی یک پایه قوی با یک پایه ضعیف [e.g. F7, failure of cyanide ion to displace OR from an ester) or 3) competing electrophilic sites (e.g. reactions of enones, where both [1,2] و [1,4] اضافه شدن امکان پذیر است).
مرحله صفر: تشکیل پایه مزدوج (اگر قبلا انجام نشده باشد). اکثر نوکلئوفیل های آنیونی به شکل آنیونی خود “ارائه می شوند”، اما انولات ها یک استثنای برجسته هستند. اگر مکانیسم یک واکنش مبتنی بر پایه مانند آلدول یا کلایزن را می نویسید، معمولاً برای شروع به شما کتون یا استر خنثی داده می شود. کتون ها، استرها و سایر ترکیبات کربونیل به خودی خود هسته دوست های ضعیفی هستند و با اکثر الکتروفیل ها به هر شکل معنی دار واکنش کندی دارند. با این حال، پس از درمان با یک پایه به اندازه کافی قوی، الگوی واکنش آنها دستخوش تغییر شدید می شود: تشکیل پایه مزدوج آنها (انولات) آنها را به هسته دوست های بسیار قوی تبدیل می کند. بنابراین مطمئن شوید که می دانید چگونه تبدیل یک ترکیب کربونیل را به انولات آن بکشید.
خوب. بنابراین بیایید امروز به دو مورد اول نگاه کنیم (آنها بسیار رایج ترین هستند) و دفعه بعد با سه مورد دیگر به پایان برسانیم.
مورد 1: [1,2]-افزودن / پروتوناسیون
الکتروفیل های مربوطه: آلدهیدها، کتونها.
نوکلئوفیل های مربوطه: گریگناردها، انولاتها، سیانیدها، آلکوکسیدها، هیدروکسیدها، هیدریدها.
مفاهیم مهمی که باید بدانید: 1) درک کنید که چگونه عوامل فضایی بر سرعت افزودن نوکلئوفیل ها تأثیر می گذارد (یعنی مانع آن می شود). 2) درک کنید که چگونه عوامل الکترونیکی بر الکترون دوستی کربونیل ها تأثیر می گذارند (یعنی کربونیل های فقیر از الکترون واکنش پذیرتر هستند؛ رتبه بندی نسبی کربونیل ها را یاد بگیرید، از فقیر الکترون تا غنی از الکترون).
مثال ها: واکنش آلدول، تشکیل سیانوهیدرین.
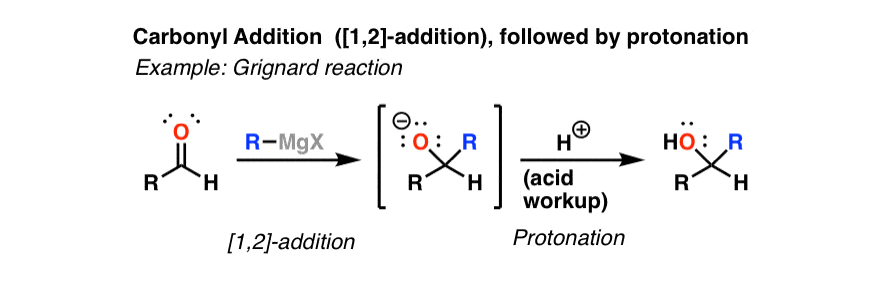
این یک نوع واکنش بسیار ساده و آشناست. هنگامی که یک هسته دوست به یک کربونیل حمله می کند تا یک ترکیب چهار وجهی ایجاد کند، واکنش نامیده می شود [1,2]-افزودن برای واکنش آلدئیدها و کتونها با هستههای آنیونی، نمودار به شرح زیر است: هسته دوست به کربونیل حمله میکند تا یک آلکوکسید چهار وجهی ایجاد کند. آلکوکسید پروتونه می شود. پایان.
تمام افزودههای نوکلئوفیلهای آنیونی به آلدئیدها و کتونها در این جدول از این طرح پیروی میکنند. بعدی وجود ندارد [1,2]- حذف، همانطور که به زودی در مورد آن بحث خواهیم کرد: آلکوکسید چهار وجهی، پس از تشکیل، فقط در محلول می نشیند تا زمانی که پروتونه شود (معمولاً از طریق آب یا خاموش کردن اسید خفیف). در [1,2]-مسیر حذف برای بازسازی کربونیل رخ نمی دهد زیرا این امر شامل بیرون راندن بازهای بسیار قوی (یعنی گروه های ترک بد) هیدرید (pKa~35) یا آلکیل (pKa~50) می شود.
مورد 2: [1,2]-افزودن به دنبال آن [1,2]-حذف.
الکتروفیل های مربوطه: کلریدهای اسید، انیدریدها، استرها
نوکلئوفیل های مربوطه: گریگناردها، انولاتها، آلکوکسیدها، هیدروکسیدها، هیدریدها.
مفاهیم مرتبط: همه چیز برای [1,2]-افزودن (بالا) به علاوه دانش توانایی های گروه ترک نسبی (به جدول pKa مراجعه کنید).
مثال ها: تراکم کلایزن، صابونی شدن، ترانس استریفیکاسیون.
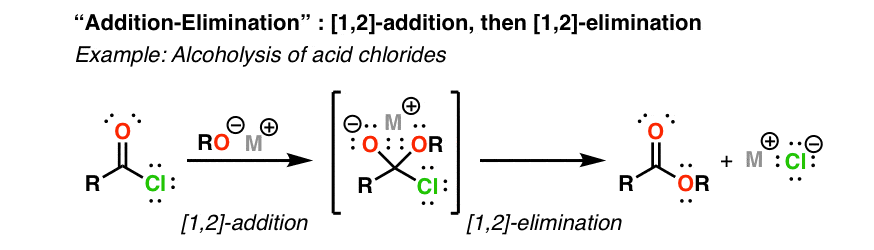
این واکنش ها با گذشتن از [1,2]-افزودن همانطور که در بالا ذکر شد برای تشکیل یک آلکوکسید چهار وجهی. با این حال، اگر گروه دیگری روی کربن وجود داشته باشد که بتواند به عنوان یک گروه خروجی مناسب در نیمه راه عمل کند، این می تواند توسط اکسیژن آنیونی در فرآیند تشکیل مجدد پیوند دوگانه کربن-اکسیژن (پیوند π) جابجا شود. این اثر تغییر گروه های عاملی در کربونیل را دارد: برای مثال، واکنش کلریدهای اسید با آلکوکسیدها برای تهیه استرها. به این می گویند [1,2]-حذف.
یک قانون بسیار سختگیرانه بر این فرآیند حاکم است. درست همانطور که حد وسط چهار وجهی در [1,2]-افزودن تجزیه نمی شود تا آنیون های H یا R آزاد آزاد کند، بازهای ضعیف تر، بازهای قوی تر را از کربونیل جابجا نمی کنند. بنابراین آگاهی از مقادیر pKa برای پیش بینی نتیجه آنها ضروری است. برای مثال، برخی از مقادیر pKa مرتبط (pKa اسید مزدوج در پرانتز): R2N- (~35)، RO (~17)؛ AcO (~4)؛ Cl (-7). آلکوکسید (RO) می تواند جایگزین AcO و Cl شود، اما نه R2N. فقط به یاد داشته باشید که یک پایگاه ضعیف نمی تواند جایگزین یک پایگاه قوی تر شود، همانطور که (در صورت عدم وجود رشوه هایی که تولید ناخالص داخلی ایتالیا را تقریب می زند) تیم فوتبال دختران نوجوان تیم بیتس پسر عموی 7 ساله من هرگز و هرگز نمی تواند آث میلان را در یک مسابقه فوتبال شکست دهد.
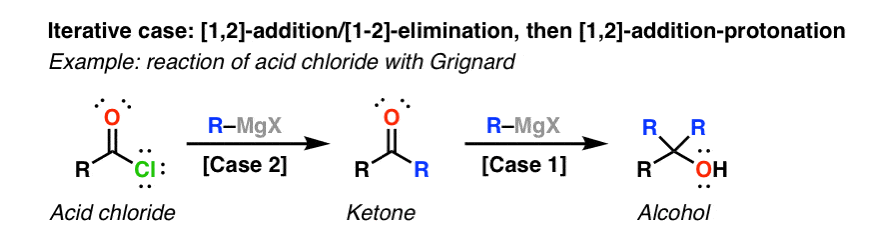
گاهی اوقات گونه های کربونیل جدید تولید شده هنوز تحت شرایط واکنش نشان می دهند و با فرض وجود هسته دوست های اضافی تحت واکنش های بیشتری قرار می گیرند. یک مثال در واکنش گریگنارد روی هالیدهای اسیدی است. افزودن گریگنارد به هالید اسیدی باعث ایجاد کتون می شود. سپس کتون به منیفولد 1،2-افزودن/پروتوناسیون قیف میشود.
من به 3 مورد باقی مانده در قسمت دوم می پردازم.
