دکتری استاد راهنما دکتری من. یک بار از ناظر نقل شده است که گفت:اساساً، تمام واکنشهای شیمی آلی به حملات هستهدوست به الکتروفیل خلاصه میشوند”
برای یک دقیقه به این موضوع فکر کنید. هنگامی که مفهوم هسته دوست خود را فراتر از گونه هایی گسترش دهید که با یک آلکیل هالید در واکنش SN2 واکنش می دهند و شامل آروماتیک ها و آلکن ها نیز می شود، تقریباً هر واکنشی که در شیمی آلی مقدماتی یاد می گیرید از این اصل پیروی می کند.
واکنش های پایه اسیدی – نوکلئوفیل (باز) به الکتروفیل (اسید) حمله می کند.
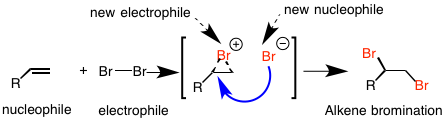
بروماسیون: نوکلئوفیل (آلکن) به الکتروفیل (برم) حمله می کند تا یک الکتروفیل جدید (یون برومونیوم) و یک هسته دوست جدید (یون برمید) ایجاد کند که بیشتر واکنش نشان می دهد و دیبرومید مجاور شما را می دهد. برای این موضوع، به تمام واکنش های افزودن آلکن نگاه کنید: آلکن (هسته دوست) به علاوه الکتروفیل های BH3، H2SO4، Hg(OAc)2، OsO4، ازن، و غیره.
صنایع فریدل و واکنشهای مرتبط نمونه دیگری هستند: نوکلئوفیل (آروماتیک) به الکتروفیل (آلکیل یا آسیل کربوکاتیون که از طریق افزودن FeCl3 یا AlCl3 ایجاد میشود) حمله میکند.

به واکنش آلدول نگاه کنید: نوکلئوفیل (انولات) به الکتروفیل (آلدئید) حمله می کند. انولات ها نوکلئوفیل های همه کاره هستند. بخشی از چالش تسلط بر شیمی کربونیل درک این است که چگونه “طعم” انولات های هسته دوست و کربونیل های الکتروفیل با تنظیم گروه های عاملی در کنار کربونیل ها تغییر می کند.

حتی واکنش دیلز-آلدر را نیز می توان در این زمینه در نظر گرفت: دین (نوکلئوفیل) به دی انوفیل (الکتروفیل) حمله می کند.

به عبارت فنی تر، آنچه که در همه این موارد توضیح داده شد، تشکیل پیوندهای جدید توسط همپوشانی اوربیتال مولکولی اشغال شده (HOMO) هسته دوست با کمترین اوربیتال مولکولی اشغال نشده (LUMO) الکتروفیل است. به طور خلاصه، ماهیت بیشتر واکنشها در شیمی آلی شامل جریان الکترونها از مکانهای غنی از الکترون (هسته دوست) به مکانهای فقیر از الکترون (الکتروفیل) است.
آیا می توانید استثنایی فکر کنید؟
