درک “الکترون ها کجا هستند” برای درک اینکه چرا واکنش ها به روش آنها اتفاق می افتد ضروری است
یک نکته از بحث طنین کم بوده است. چه فایده ای دارد؟
چه کسی اهمیت می دهد که بتوانیم ساختارهای رزونانس را بنویسیم؟ چه اهمیتی دارد که بتوانیم دو یا سه ساختار رزونانسی پایدار را کشف کنیم؟ پس چی؟
1. درک چگونگی تعیین چگالی الکترون به این معنی است که شما کمتر به حفظ تکیه خواهید کرد و می توانید رفتار شیمیایی مولکول هایی را که قبلاً ندیده اید کشف کنید.
نکته اینجاست: ما می توانیم از رزونانس (و الکترونگاتیوی) برای کشف چگالی الکترونی مولکول ها از اصول اولیه استفاده کنیم. و ما میتوانیم این چگالی الکترونها را برای درک چگونگی واکنش یک مولکول به کار ببریم.
به عبارت دیگر: اگر این مهارت را یاد بگیرید، متکی خواهید شد کمتر در حفظ کردن برای درک واکنش ها، زیرا میتوانید رفتار شیمیایی مولکولهایی را که قبلاً ندیدهاید، کشف کنید.
به عنوان مثال: اگر شما یک رشته غیر شیمی هستید، تقریباً می توانم تضمین کنم که قبلاً چنین واکنشی را ندیده اید. اما اگر برخی از اصول موجود در این پست را به کار ببرید، باید بتوانید در آن پیشرفت هایی داشته باشید.
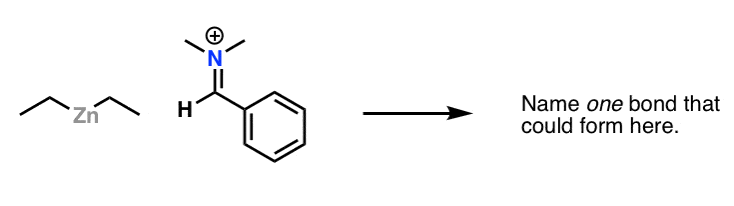
بیایید به سرعت به این دو جنبه نگاه کنیم.
2. استفاده از الکترونگاتیوها برای درک چگالی الکترونی یک مولکول
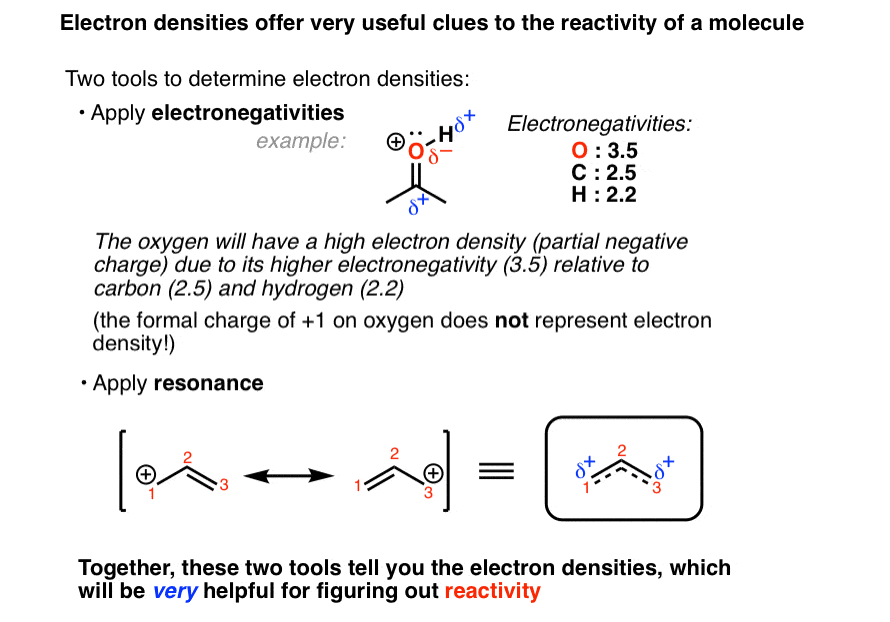
استفاده از الکترونگاتیوی وقتی بین دو اتم با الکترونگاتیوهای مختلف پیوند برقرار کنید، یک دوقطبی (دو بار مخالف در فضا از هم جدا می شوند) وجود خواهد داشت. آن دوقطبی به شما سرنخی در مورد چگالی الکترون آن دو اتم می دهد. به عنوان مثال در مولکول زیر، اکسیژن بیشتر از کربن الکترونگاتیو است، به این معنی که پیوند C-O به سمت اکسیژن قطبی می شود (چگالی الکترونی بالاتری خواهد داشت). این با هزینه رسمی متفاوت است، جایی است که ما باید برای اهداف «حسابداری» به یک اتم شارژ اختصاص دهیم.
3. استفاده از تشدید برای درک چگالی الکترون یک مولکول
استفاده از رزونانس: هنگامی که پایدارترین دو (یا سه) فرم تشدید را بشناسید، ایده خوبی از رزونانس خواهید داشت. ترکیبی به نظر می رسد. هیبرید رزونانس همچنین چگالی الکترون را به شما می گوید، گاهی اوقات به روشی که بلافاصله از الکترونگاتیوی آشکار نیست (به زیر مراجعه کنید).
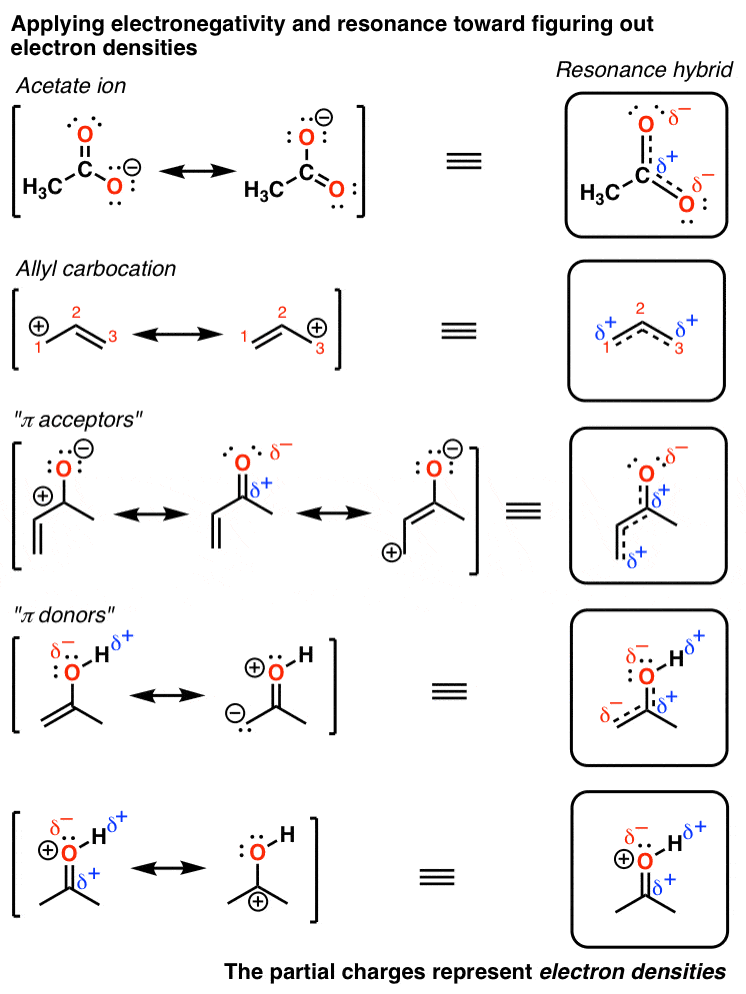
4. چند نمونه از هیبریدهای تشدید
در اینجا چند نمونه از هیبریدهای تشدید، همراه با چگالی الکترونی که از اعمال به دست می آوریم، آورده شده است هر دو الکترونگاتیوی و رزونانس در تصویر، بارهای جزئی (δ) نشان دهنده چگالی الکترون در هیبرید است.
حالا برای خط پانچ.
5. استفاده از این دو عامل برای کشف واکنش پذیری شیمیایی: مناطق با چگالی الکترون بالا به دنبال مناطق با چگالی الکترونی پایین خواهند بود.
هنگامی که بارهای جزئی یک مولکول را می دانید، می توانید از آن برای کشف کردن استفاده کنید واکنش شیمیایی قابل قبول چطور؟
“خلاصه یک جمله شیمی” را به خاطر بسپارید: بارهای مخالف جذب می شوند، مانند دفع بارها.
بنابراین هر منطقه از بار منفی روی یک مولکول درجاتی از جاذبه به a خواهد داشت منطقه بار مثبت روی یک مولکول دیگر
در واکنشها، الکترونها از مناطقی از چگالی الکترون بالا به چگالی الکترون کم راه دیگری برای قرار دادن آن: بار منفی جزئی (یعنی چگالی الکترون بالا) به ناحیه ای با بار مثبت جزئی (یعنی چگالی الکترون کم) می رود.
بنابراین در نمودار زیر برخی از هیبریدهای تشدید (همراه با مولکولهای دیگر) را آوردهام و مجموعهای از برهمکنشهای بین بارهای مخالف را ترسیم کردهام. اگرچه این فلش ها لزوماً نشان نمی دهند واقعی واکنشها (اگرچه خیلیها این کار را میکنند!) حداقل نشان میدهند واکنش های بالقوه امکان پذیر
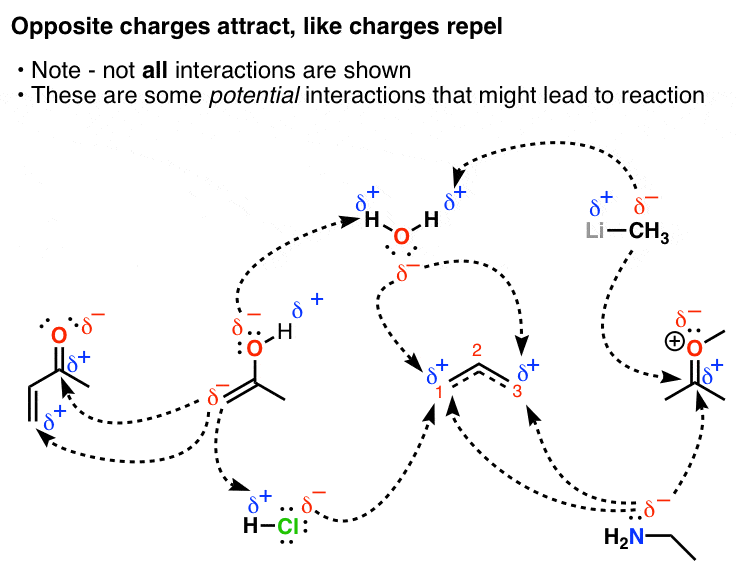
مهارت کلیدی از این مثالها این است که بتوانیم ببینیم چگونه ترکیب رزونانس چگالی الکترون را تعیین میکند و چگونه میتواند منجر به فرضیههایی برای واکنشهای امکانپذیر شود.
6. بازگشت به سوال اصلی
برگردیم به سوال اصلی:
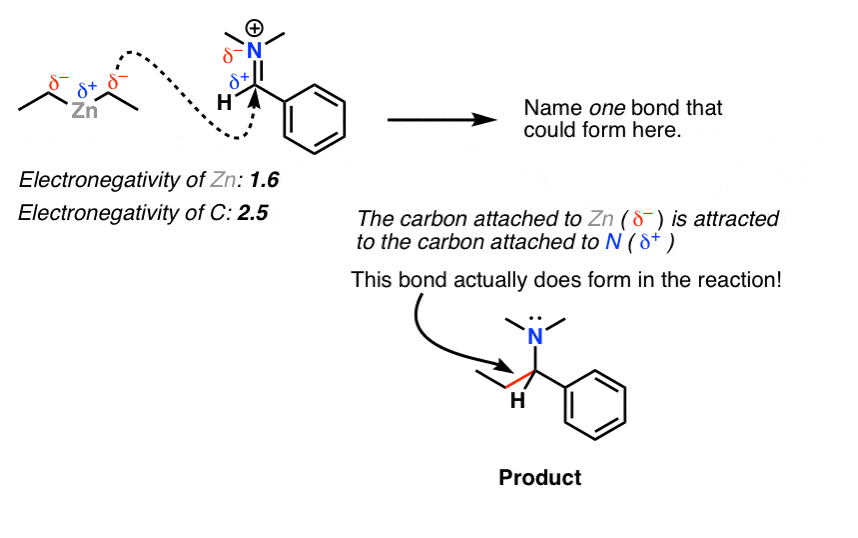
با اعمال الکترونگاتیوی، میتوانیم قضاوت کنیم که پیوند C-Zn به سمت کربن قطبی میشود که آن را غنی از الکترون میکند. باید به سمت کربن مولکول دوم جذب شود، که هم الکترونگاتیوی و هم تشدید به ما می گویند که باید یک بار مثبت جزئی داشته باشد.
در واقع این است هر چند یک واکنش واقعی ما نمی توانیم به طور کامل تعیین کنیم که یک واکنش چقدر خوب از اصول اولیه کار می کند. شواهد تجربی یک و تنها داور در مورد اینکه آیا یک واکنش موثر است یا خیر است.
آیا این تکنیک بدون استثنا کامل است؟ خیر کامل نیست. کاملاً بدون استثنا نیست. [Note 1]
اما این یک مدل ذهنی خوب برای اصول اساسی واکنش شیمیایی است. نکته اینجاست که به شما نگاهی اجمالی به نحوه بکارگیری مفاهیم الکترونگاتیوی و تشدید در موقعیت های جدید و ناآشنا بدهیم.
7. برخی از واکنش هایی که هرگز رخ نخواهند داد
یک پست به اندازه کافی طولانی است، اما در اینجا برخی از تعاملات “غیرمولد” از نمودار بالا آورده شده است.
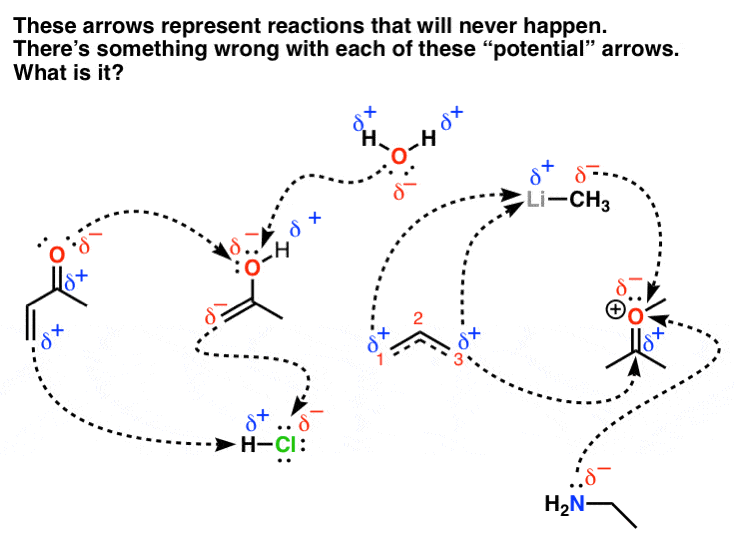
یادداشت
یادداشت 1. دو استثنای برجسته: الکترونگاتیوی برای پی بردن به واکنش پذیری یون نیتریل (CN(-) و oxymercuration آلکن ها بهترین نیست. واکنش پذیری Cl-Cl و Br-Br و غیره را که قطبی نیستند پیش بینی نمی کند.
تبصره 2. توجه داشته باشید که این مدل به شما نمی گوید چگونه گونه های مختلف واکنشی خواهند بود. این به مجموعه دیگری از مدل های ذهنی نیاز دارد.
