گروههای استوایی در مقابل گروههای محوری: چرا موقعیت استوایی انرژی کمتری دارد
فقط برای اینکه شما را به سرعت بالا ببریم، اجازه دهید به سرعت آخرین پست را مرور کنیم. و در پایین، من یک فیب کوچک را که در پست آخر ساخته بودم، اصلاح می کنم.
1. بررسی مختصر در مورد ساختار صندلی سیکلوهگزان
1. سیکلوهگزان تحت یک تبدیل ساختاری قرار می گیرد که به عنوان چرخش صندلی شناخته می شود. در این چرخاندن صندلی، همه گروه های محوری استوایی می شوند و همه گروه های استوایی محوری می شوند. [but all “up” groups remain up, and all “down” groups remain down].
2. دو شکل صندلی خود سیکلوهگزان کاملاً غیرقابل تشخیص هستند، اما این در بیشتر موارد درست نیست.. به عنوان مثال، در 1-متیل سیکلوهگزان، یک کانفورمر صندلی دارای یک محوری گروه متیل و در دیگری گروه متیل است استوایی. اینها ایزومرهای ساختاری یا به طور ساده “کنفرم کننده” هستند.
3. در دمای اتاق، این دو ترکیب به سرعت با یکدیگر در تعادل هستند. یک سد فعال سازی در حدود 10 کیلوکالری در مول برای این تبدیل وجود دارد، زیرا کنفورمر “نیمه صندلی” با انرژی بالا یک واسطه در این فرآیند است. تلاش برای مشاهده هر دو ترکیب 1-متیل سیکلوهگزان در دمای اتاق با دستگاهی برای گرفتن “عکس های فوری مولکولی” (طیف سنج NMR همان چیزی است که ما استفاده می کنیم – جزئیات دقیق تر در این مورد در پست های بعدی) منجر به تار شده تصویر مانند یک دوربین قدیمی که سعی می کند از پره های چرخ دوچرخه متحرک عکس بگیرد، “سرعت شاتر” بسیار آهسته است و نتیجه این است که تصاویر با هم ترکیب می شوند تا میانگینی را ارائه دهند. با استفاده از این دستگاه، نمی توان هر دو کنفورمور سیکلوهگزان 1-متیل سیکلوهگزان را در دمای اتاق مشاهده کرد.
4. در دمای بسیار پایین (حدود 80 درجه بالای صفر مطلق) تعادل بین دو شکل صندلی متوقف می شودزیرا انرژی حرارتی کافی برای بالا رفتن از سد فعال سازی 10 کیلوکالری در مول وجود ندارد. اکنون، وقتی میخواهیم «عکسهای فوری مولکولی» از 1-متیل سیکلوهگزان بگیریم، ما در واقع این دو ترکیب را جداگانه می بینیم.
حالا، اصلاح فیب.
در پست آخر فرض کردیم که این دو ترکیب از نظر انرژی با هم برابر باشند و بنابراین شاهد مخلوطی 50:50 از این دو خواهیم بود.
آیا این درسته؟
2. در 1-متیل سیکلوهگزان، نسبت کنفورمر متیل استوایی به متیل کنفورمر محوری 95:5 است.
فقط یک راه برای فهمیدن وجود دارد. آزمایش را با یک سیکلوهگزان جایگزین مانند 1-متیل سیکلوهگزان انجام دهید.
وقتی این کار را انجام میدهیم، این چیزی است که مییابیم. به جای مساوی بودن، نسبت کنفورمرهای “متیل استوایی” به “متیل محوری” حدود ** است. 95:5 به نفع ترکیبی که در آن گروه متیل استوایی است.
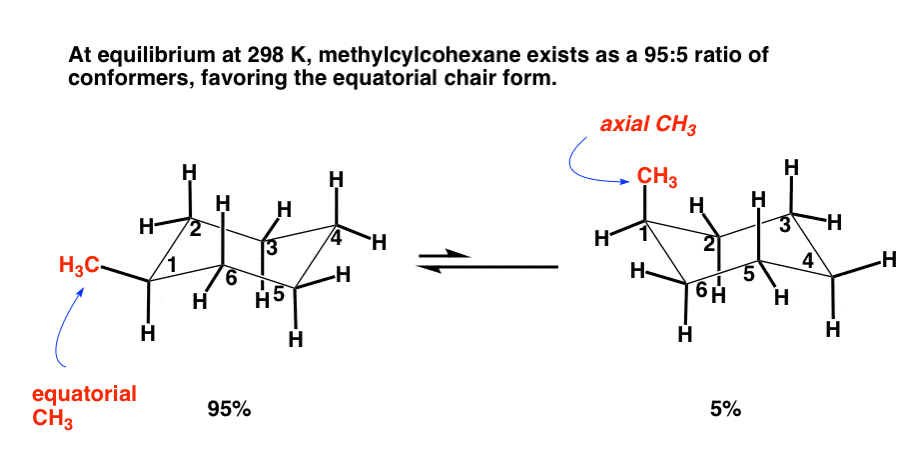
بسیار جالب! این باید به این معنی باشد که ترکیب استوایی انرژی کمتری نسبت به ترکیب “محوری” دارد.
چرا ممکن است؟
3. ترکیب متیل “استوایی” با برهمکنش های گاوش کمتری نسبت به ترکیب متیل محوری مواجه می شود.
بیایید به طرح نیومن صندلی نگاه کنیم. تصور کنید در امتداد پیوند C-1 به C-2 (که همسطح با پیوند C-4 به C-5 است) نگاه کنید. این چیزی است که می بینید.
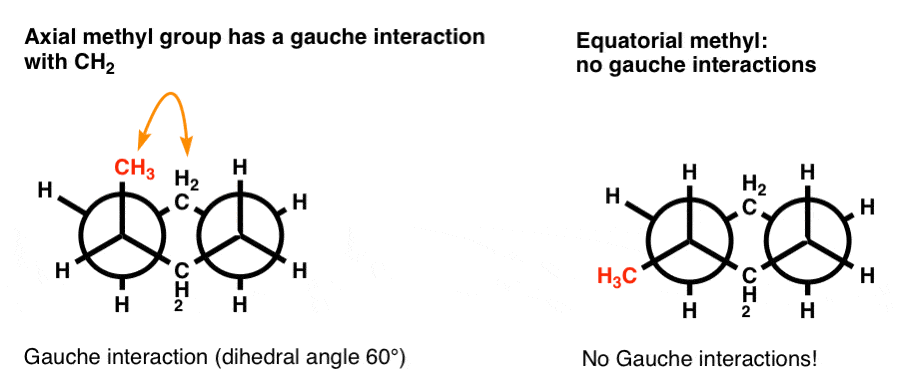
توجه داشته باشید که در ترکیبی که متیل محوری است، یک برهمکنش گاوش بین گروه متیل محوری و C-3 وجود دارد. این هست غایب در ترکیبی که متیل استوایی است. این برهمکنش گاوش نمونهای از کرنش واندروالس است که باعث میشود کنفورمور محوری انرژی بیشتری داشته باشد.
در واقع یک وجود دارد دومین اگر در امتداد C-1 تا C-6 نگاه کنید، تعامل گاوش. این تعامل گاوش با C-5 است.
یک راه ساده برای پیگیری این است که آن را به عنوان گروه متیل در نظر بگیریم که با هیدروژن های دیگر «محوری» در C-3 و C-5 در تعامل است. اینها “برهمکنش های دو محوری” نامیده می شوند زیرا برهمکنش های فضایی بین جانشین های محوری هستند.
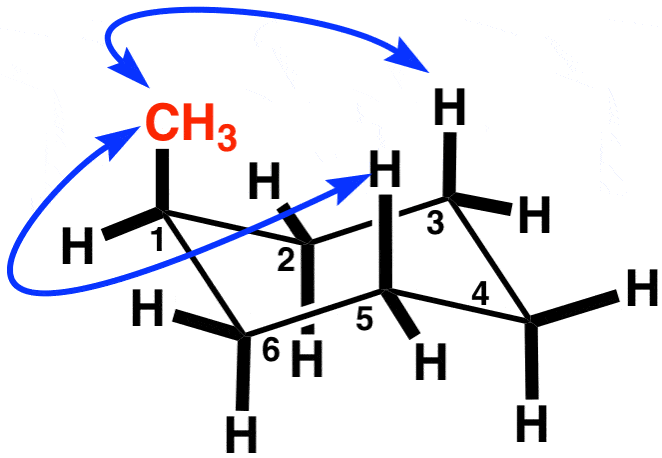
خط پایین: در دو ترکیب نابرابر از یک حلقه سیکلوهگزان، ترکیبی که در آن فعل و انفعالات فضایی به حداقل می رسد مطلوب خواهد بود. **
4. نسبت تعادلی تعیین شده تجربی کنفورمرها می تواند برای محاسبه اختلاف انرژی استفاده شود
حالا در اینجا یک نتیجه شسته و رفته از این دانش است. از آنجایی که این نسبت کنفورمورها (95:5) سیستمی را در حالت تعادل نشان می دهد، ما در واقع می توانیم از آن برای محاسبه استفاده کنیم. تفاوت در انرژی از این دو کنفورمر با استفاده از معادله زیر:
![]()
برای مخلوط 50:50 (K = 1) اختلاف انرژی ΔG صفر خواهد بود.
برای متیل سیکلوهگزان در دمای اتاق (298 کلوین) نسبت 95:5 کانفورمرهای استوایی به محوری به تفاوت انرژی تبدیل می شود. 1.70 کیلو کالری در مول.
به عبارت دیگر، کانفورمر استوایی 1.70 کیلوکالری در مول پایدارتر است.
از آنجایی که دو برهمکنش گاوش وجود دارد و انرژی کرنش 1.70 کیلوکالری در مول است، محاسبه مقدار هر برهمکنش آسان است: 0.85 کیلوکالری در مول.
5. خلاصه: گروه های محوری در مقابل استوایی
حالا این همه نوع سوال را باز می کند. اگر یک گروه متیل (CH3) منجر به اختلاف انرژی 1.70 کیلوکالری در مول می شود، پس یک گروه اتیل (CH) چه تاثیری خواهد داشت.2CH3) دارند؟ یا کلر؟ یا اوه؟ یا ترت بوتیل؟
میتوانیم از همین رویکرد برای اندازهگیری همه این اعداد استفاده کنیم. اطلاعات بیشتر در مورد آن در پست بعدی
یادداشت
* این کمی تقلب است. در معادله ΔG = –RT ln K، مقدار K به T مربوط می شود، بنابراین نسبت تعادل در 80- درجه سانتی گراد کمی متفاوت از مقدار در دمای اتاق خواهد بود. [quiz time – do you think it will be higher than 95:5 or lower than 95:5 ?] با این حال، سپس میتوان ΔG را حل کرد و از این عدد برای محاسبه K در دمای اتاق استفاده کرد.
** دانشجویان کارآفرین ممکن است بپرسند اگر هیدروژن های محوری C-3 و C-5 حذف شوند چه اتفاقی می افتد. آیا این تعادل را تغییر می دهد؟ کاملا!
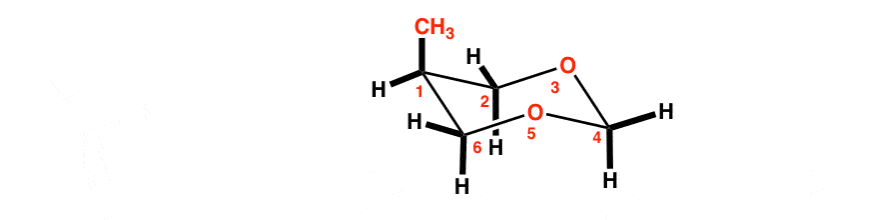
در مولکول بالا، CH2 گروه های C-3 و C-5 با اکسیژن جایگزین شده اند. از آنجایی که دیگر هیچ برهمکنش دو محوری قابل توجهی بین گروه متیل و جانشین های روی حلقه وجود ندارد، تفاوت انرژی قابل توجهی بین ترکیبات استوایی و محوری این مولکول وجود ندارد.
(پیشرفته) مراجع و مطالعه بیشتر
این موضوعی است که معمولاً در مقطع کارشناسی در شیمی آلی تدریس می شود و همراه با بحث در مورد آ-ارزش های. جانشین ها در سیکلوهگزان می توانند دو موقعیت محوری و استوایی داشته باشند و ارجح ساختار توسط اثرات استریو الکترونیکی دیکته می شود.
- بررسی های پراش الکترونی ساختارهای مولکولی. II. نتایج به دست آمده با روش بخش چرخشی.
هاسل، او. ویرول، اچ.
Acta Chem. Scand. 1947، 1، 149-168
DOI: 3891/acta.chem.scand.01-0149 - ساختار مولکول های حاوی حلقه های سیکلوهگزان یا پیرانوز.
هاسل، او. اوتار، بی.
Acta Chem. Scand. 1947، 1، 929-943
DOI: 3891/acta.chem.scand.01-0929
Odd Hassel برای اولین بار تایید کرد که سیکلوهگزان در حال حاضر معمولاً پذیرفته شده وجود دارد صندلی تائیدیه. او همچنین پیشنهاد کرد که جانشینها میتوانند دو نوع موقعیت متفاوت روی حلقه بگیرند که آنها را پیوندهای c و e-e-باند نامید. او همچنین نشان داد که آنالیز ساختاری سیکلوهگزانها را میتوان به سایر حلقههای 6 عضوی غیراشباع، مانند پیرانوزهایی که معمولاً در کربوهیدراتها یافت میشود، گسترش داد. Odd Hassel بعداً جایزه نوبل شیمی را با پروفسور DHR Barton به خاطر کارش در مورد تجزیه و تحلیل ساختاری به اشتراک گذاشت. - خواص ترمودینامیکی و ساختار مولکولی سیکلوهگزان، متیل سیکلوهگزان، اتیل سیکلوهگزان و هفت دی متیل سیکلوهگزان
چارلز دبلیو بکت، کنت اس پیتزر و رالف اسپیتزر
مجله انجمن شیمی آمریکا 1947، 69 (10)، 2488-2495
DOI: 1021/ja01202a070
این مقاله ابتدا اصطلاحات «قطبی» و «استوایی» را برای دو نوع موقعیتی که جانشینها میتوانند در سیکلوهگزان بگیرند، پیشنهاد میکند. - نامگذاری از سیکلواوراق قرضه هگزانی
بارتون، دی.، هاسل، او.، پیتزر، ک.، پرلوگ، وی.
طبیعت 1953، 172، 1096-1097
DOI: 1038/1721096b0 - نامگذاری پیوندهای سیکلوهگزانی
HR Barton، O. Hassel، KS Pitzer، V. Prelog
علوم پایه 1954، 119، 49
DOI: 10.1126/science.119.3079.49
اینها اولین مواردی هستند که از اصطلاحات «محوری» و «استوایی» برای نشان دادن دو موقعیتی که جانشینها میتوانند در سیکلوهگزان بگیرند استفاده میشود. این نیز به زمانی برمیگردد که دانشمندان میتوانستند با خیال راحت به انتشار متقابل بپردازند تا دید بهتری داشته باشند – تقریباً همان مقاله در هر دو منتشر شده است. علوم پایه و طبیعت، مجلات برتر محسوب می شوند. - همسایگی کربن و هیدروژن. نوزدهم مشتقات t-Butylcyclohexyl. تحلیل ساختاری کمی
وینستین و نی جی هولنس
مجله انجمن شیمی آمریکا 1955، 77 (21)، 5562-5578
DOI: 10.1021/ja01626a037
این مقاله ای است که برای اولین بار مفهوم آن را معرفی کرد آ-مقادیر (به جدول XII مراجعه کنید) و نحوه تعیین آنها از طریق اندازهگیریهای جنبشی (solvolytic)، چیزی که پروفسور وینستین به آن معروف بود. مقدمه خلاصه ای از چگونگی را نشان می دهد آ– ارزشها تعیین میشوند و بعداً پروفسور وینستین میگوید:مقدار انرژی که توسط آن یک گروه t-butyl موقعیت استوایی را ترجیح می دهد به اندازه کافی بزرگ است تا همگنی ساختاری را برای اکثر مشتقات 4-t-butylcyclohexyl تضمین کند.”، که امروزه معمولا در کلاس های شیمی آلی تدریس می شود. - مطالعات نرخ تبدیل و جمعیتهای ساختارهای مختلف ترکیبات حلقه اشباع شده توسط NMR: I. کلروسیکلوهگزان و بروموسیکلوکسان
دبلیو ریوز، KO Strømme
مجله شیمی کانادا، 1960، 38 (8): 1241-1248
DOI: 10.1139/v60-176
این ممکن است اولین مقالهای باشد که واقعاً از NMR برای تعیین نسبتهای محوری: استوایی سیکلوهگزانهای جایگزین استفاده میکند. با این حال، نویسندگان به صراحت محاسبه نمی کنند آ-ارزشها در اینجا، به همین دلیل است که این مقاله در مقایسه با مقاله کمتر شناخته شده است JACS انتشار جنسن، بوشولر، و بک در زیر. - تجزیه و تحلیل ساختاری – مشارکت های بنیادی DHR Barton و O. Hassel
مباحث مربوط به استریوشیمی 1967، 1، 1-17
DOI: 10.1002/9780470147153.ch1
خلاصه ای از مقالات کلیدی که پروفسور. بارتون و هاسل در تجزیه و تحلیل تاییدی منتشر کردند و جایزه نوبل شیمی را در سال 1969 به دست آوردند. - ترجیحات ساختاری در سیکلوهگزان های تک جایگزین تعیین شده توسط طیف سنجی رزونانس مغناطیسی هسته ای
فردریک آر. جنسن، سی. هکت بوشولر، و باربارا اچ. بک
مجله انجمن شیمی آمریکا 1969، 91 (2)، 344-351
DOI: 10.1021/ja01030a023
این اولین مقاله ای است که در واقع مقادیر A را از طریق NMR با اندازه گیری نسبت استوایی: محوری سیکلوهگزان های تک جایگزین مختلف تعیین می کند. - تعیین تجربی انرژی آزاد ساختاری، آنتالپی و تفاوت های آنتروپی برای گروه های آلکیل در آلکیل سیکلوهگزان ها با طیف سنجی تشدید مغناطیسی کربن-13 دمای پایین
هارولد بوث و جرمی آر اورت
جی. شیمی. Soc.، Perkin Trans. 2، 1980، 255-259
DOI: 10.1039/P29800000255
این مقاله استفاده از 13C NMR برای تعیین تفاوت های انرژی آزاد بین آلکیل سیکلوهگزان های جایگزین محوری و استوایی (در اصل، آ-ارزش های).
