سنتز اسید آمینه Strecker
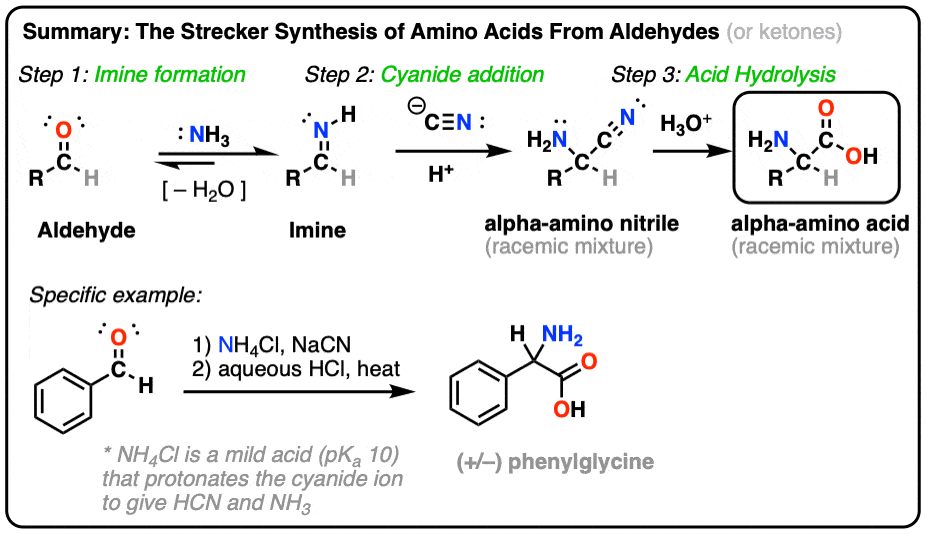
- این سنتز استرکر یک روش دو مرحله ای برای سنتز است آمینو اسید.
- با اضافه شدن شروع می شود یون سیانید به یک ایمین، تشکیل آلفا آمینو نیتریل. سپس این هیدرولیز می شود (مثلاً با اسید قوی) تا یک اسید آمینه آلفا ایجاد کند.
- با تغییر گروه R بر روی ایمین، طیف گسترده ای از آمینو اسید ممکن است به این شکل ساخته شود
فهرست مطالب
- سنتز استرکر اسیدهای آمینه
- مکانیسم دو قسمتی اسیدهای آمینه
- کاربرد: سنتز L-DOPA
- یادداشت
- (پیشرفته) مراجع و مطالعه بیشتر
1. سنتز استرکر اسیدهای آمینه
چه چیزی را در مورد یون سیانید دوست ندارید؟
باشه باشه، این یک سم کشنده است و باید در آزمایشگاه با دقت بسیار زیادی درمان شود.
ولی علاوه بر آن، این یک هسته دوست عالی است که میتواند با طیف گستردهای از الکتروفیلها واکنش نشان دهد، و در نتیجه پیوند کربن-کربن جدید به یک گروه عاملی (نیتریل) ختم میشود که میتواند به روشهای مختلف توضیح داده شود.
در زیر سه نمونه از یون سیانید در عمل آورده شده است. هنگامی که به آلکیل هالیدها اضافه می شود، نیتریل تولید می کند. به کتون ها و آلدهیدها حمله می کند و سیانوهیدرین می دهد. و همچنین به پسرعموهای نیتروژن دار آلدهیدها و کتون ها که در غیر این صورت به نام ایمین شناخته می شوند، حمله می کند. این منجر به آلفا آمینو نیتریل می شود.
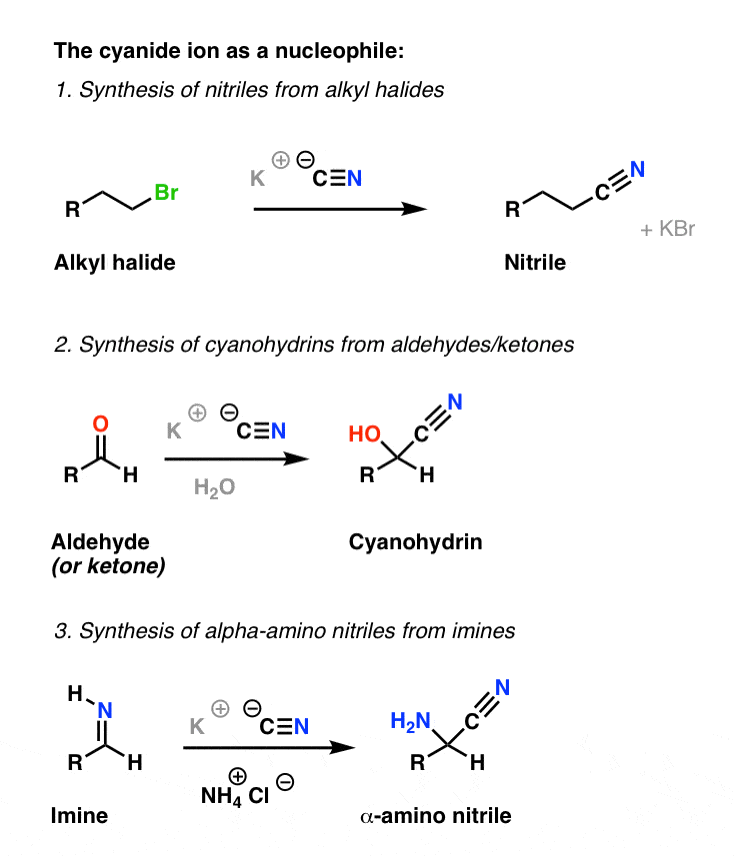
اکنون، شاید “آلفا آمینو نیتریل” نامی نباشد که به راحتی از زبان خارج شود.
اما شاید شما درباره اسیدهای آمینه شنیده باشید؟
همانطور که گفتیم، نیتریل ها می توانند به گونه های مختلفی تبدیل شوند: آمین ها (از طریق احیاء) کتون ها (از طریق افزودن یک Grignard و سپس هیدرولیز)، و مهمتر از همه برای اهداف ما، اسیدهای کربوکسیلیک (از طریق هیدرولیز اسیدی). (به پست: هیدرولیز آمیدها مراجعه کنید)
بنابراین باید انتظار داشت که هیدرولیز یک “آلفا آمینه نیتریل” با اسید آبی باعث ایجاد یک اسید آمینه آلفا (یا به اختصار فقط “اسید آمینه”) شود.
و در واقع این کار را می کند!
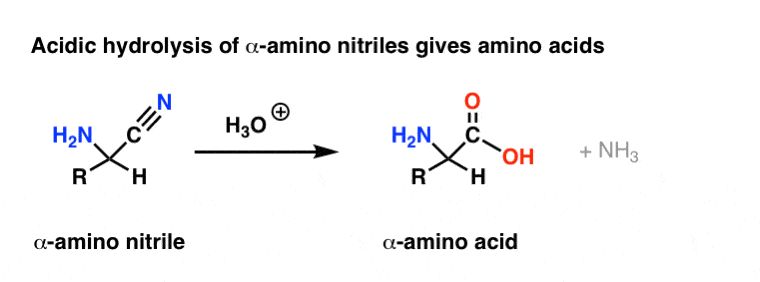
روش ساخت اسیدهای آمینه از آلدهیدها و کتون ها (از طریق ایمین ها) به عنوان سنتز استرکر از اسیدهای آمینه
بسته به گروه “R” ایمین، طیف گسترده ای از اسیدهای آمینه را می توان با استفاده از این روش سنتز کرد.
به عنوان مثال، در اینجا یک سنتز فنیل آلانین، یکی از 20 “پروتئین زا” (یعنی پروتئین سازیاسیدهای آمینه کد شده در RNA پیام رسان (mRNA):
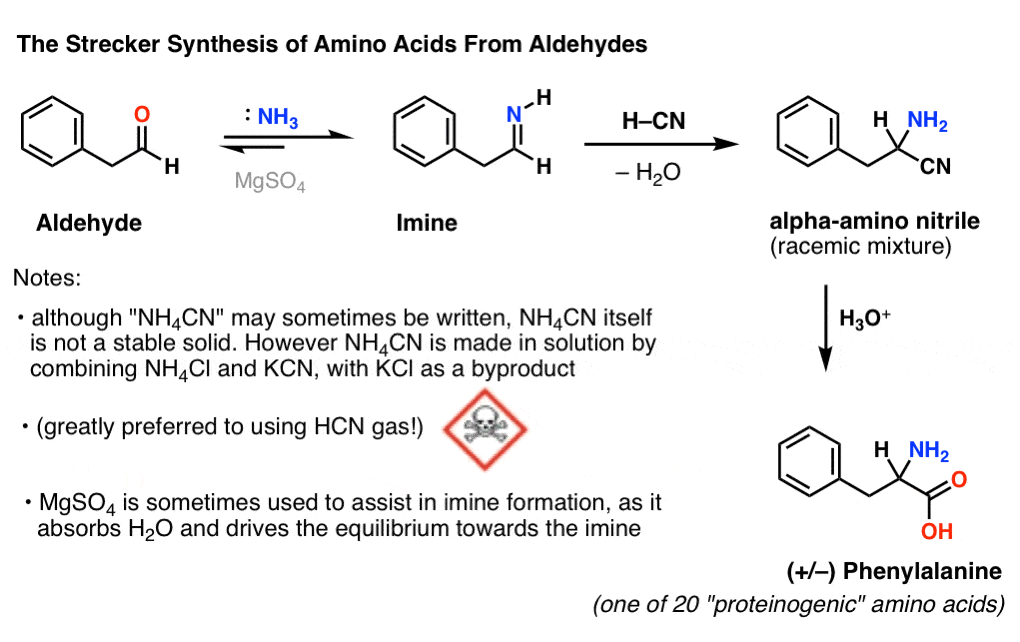
پروتکل اصلی Strecker (1850) از NH استفاده می کرد3 و هیدروژن سیانید (HCN).
با توجه به اینکه اکثر شیمیدانان علاقه کمتری به کار با گاز سیانید دارند، [Note 1] یک پروتکل ایمن تر با استفاده از مواد جامد به راحتی قابل حمل NH4کلر (کلرید آمونیوم) و KCN (سیانید پتاسیم) به طور کلی استفاده می شود [Note 2 about NH4CN]. ایده در اینجا این است که اسیدی خفیف (pKآ 9) یون آمونیوم آلدهید را پروتونه می کند و آن را برای حمله با NH آزاد شده فعال می کند.3. پس از حمله NH3، انتقال پروتون و حذف آب، یون سیانید سپس به ایمین حاصل حمله می کند (یا به احتمال زیاد اسید مزدوج ایمین، معروف به “ایمینیوم”). این منجر به آلفا آمینو نیتریل می شود.
افزودن یک نمک جاذب آب (خشک کننده) مانند MgSO4 اغلب به تشکیل ایمین کمک می کند، زیرا به ایجاد تعادل به سمت ایمین کمک می کند.
2. مکانیسم دو قسمتی سنتز استرکر
بخش اول Strecker شامل تشکیل آلفا آمینه نیتریل است که در مسیر رسیدن به اسید آمینه پروتئین زا والین (که معمولاً به اختصار Val یا V نامیده می شود) است.
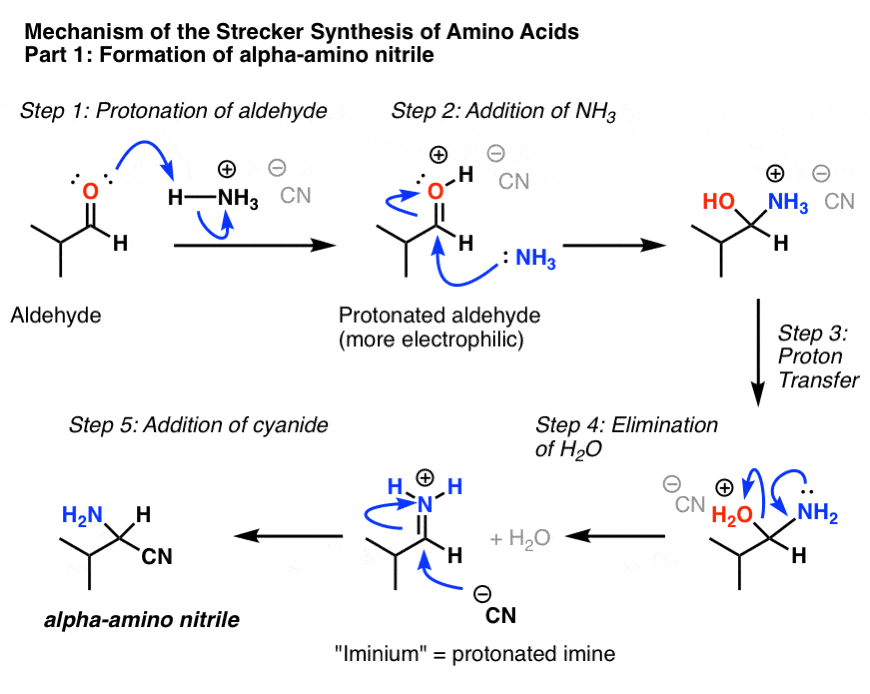
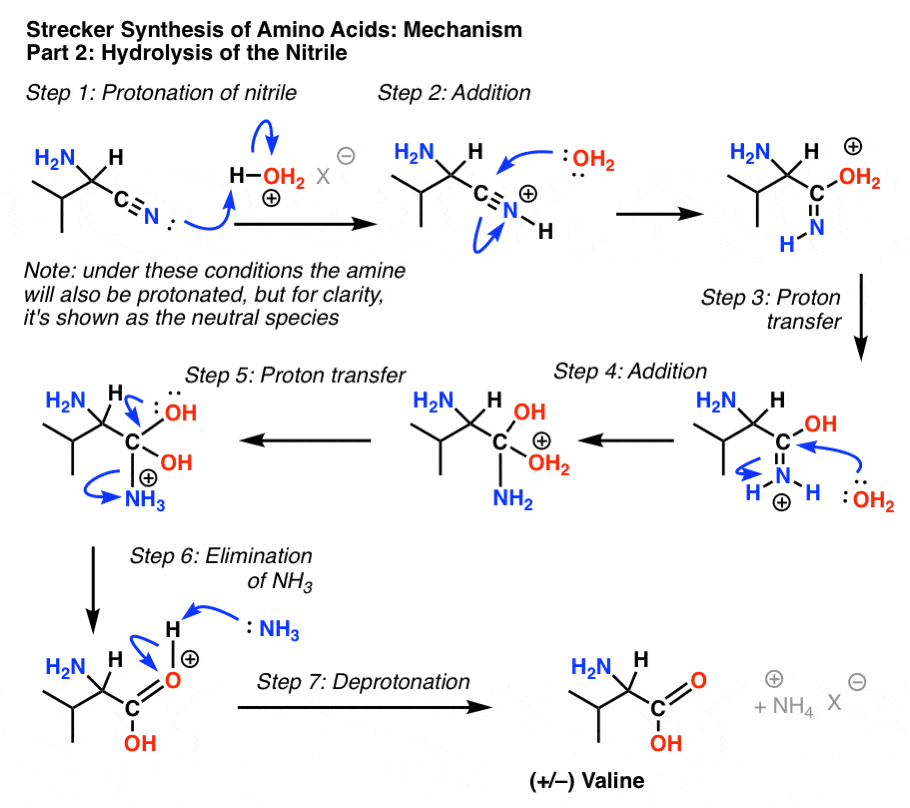
مرحله بعدی هیدرولیز نیتریل با اسید آبی است. در اینجا به صورت H نشان داده شده است3O+ با ضد یون نامشخص به عنوان X.
پروتوناسیون نیتریل (توجه: NH2 تحت این شرایط نیز پروتونه می شود، اما برای وضوح، به عنوان گونه خنثی نشان داده می شود) به دنبال آن حمله آب (مرحله 2) است. انتقال پروتون به نیتروژن (مرحله 3) و سپس افزودن آب به کربن (مرحله 4) و انتقال پروتون دیگر به نیتروژن (مرحله 5) منجر به آمونیوم با بار مثبت می شود که به عنوان NH حذف می شود (مرحله 6)3. پروتون زدایی از اکسیژن کربونیل (مرحله 7) فرآیند را کامل می کند و والین را به عنوان مخلوط راسمیک انانتیومرها می دهد.
3. سنتز یک اسید آمینه غیر پروتئین زا: L-DOPA
ممکن است بپرسید: پس چی؟
پروتئین ها (به عنوان مثال از سویا یا آب پنیر) به آسانی در دسترس هستند و آمینو اسیدهای طبیعی را می توان ارزان و به راحتی از هیدرولیز پروتئین ها جدا کرد. از آنجایی که طبیعت آنها را در چنین ذخایر فراوانی فراهم میکند، چرا برای ساختن آنها زحمت بکشیم؟
دلایل زیادی. یکی از این موارد: اسیدهای آمینه پروتئین زا اغلب به روش های مختلفی اصلاح می شوند in vivoو روشی برای دسترسی به برخی از این اسیدهای آمینه نادرتر و اصلاح شده ضروری می شود. یک مثال L-DOPA است، یک درمان مهم برای بیماری پارکینسون (در بدن به دوپامین و آدرنالین تبدیل می شود).
که در داخل بدنL-DOPA از طریق هیدروکسیلاسیون تیروزین ساخته می شود، اما شیمیدانان آلی هنوز به نحوه انجام این واکنش در آزمایشگاه تسلط کامل ندارند. یک جایگزین ایجاد L-DOPA از طریق واکنش Strecker است. شروع با 3،4-دی هیدروکسی فنیل استالدئید (زیر) با NH4CN» (ساخته شده از ترکیب NH4کلر و KCN در محلول) و به دنبال آن هیدرولیز اسیدی منجر به مخلوط راسمیک L- و D- DOPA می شود. سپس L-DOPA خالص را می توان از طریق تفکیک کایرال به دست آورد. (توجه داشته باشید که DL-DOPA همان (+/–)-DOPA است. فقط یک روش متفاوت برای به تصویر کشیدن یک مخلوط راسمیک.) [Note 3]
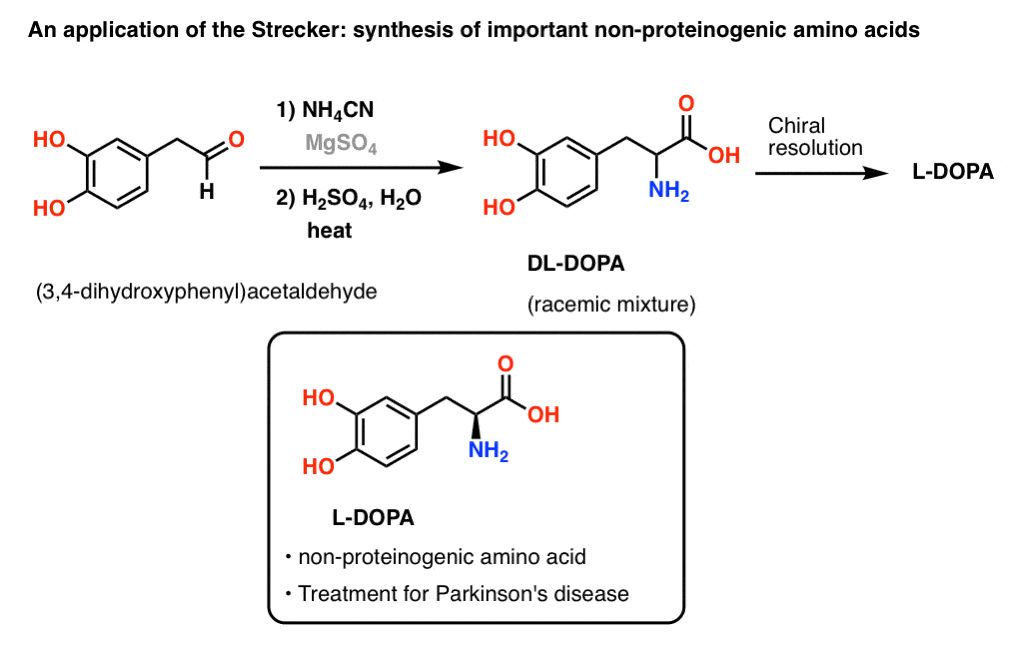
Strecker همچنین میتواند برای ساخت اسیدهای آمینه غیر طبیعی با استریوشیمی غیرطبیعی، برچسبهای فلورسنت، آزیدها (برای کاربردهای شیمی “کلیک کنید”) و بسیاری از خواص دیگر استفاده شود. این یک واکنش “حاشیه ای” نیست. Strecker مهم است.
یک هشدار: همانطور که نشان داده شده است، Strecker ارائه می دهد خوشه، شاخه اسیدهای آمینه و طبیعت از اسیدهای آمینه خالص انانتیومر استفاده می کند.
بنابراین آیا می توان Strecker را طوری تغییر داد که فقط یک انانتیومر تولید کند؟
پاسخ کوتاه بله است. یکی از اولین کاربردهای کمکی کایرال (1963!) در واکنش استرکر توسط گروه هارادا بود. در چند سال گذشته، رویکردهای نامتقارن کاتالیزوری مختلفی توسعه یافته است که خارج از محدوده بحث ما است. برای مطالعه بیشتر شما را به آثار یاکوبسن و سانگ ارجاع می دهم.
از قضا مشکل ساخت L-DOPA خالص انانتیومری نه از طریق Strecker، بلکه از طریق هیدروژناسیون کاتالیزوری که توسط Knowles و گروهش در DuPont در دهه 1970 ایجاد شد، حل شد. این برنده سهمی از جایزه نوبل شیمی سال 2001 برای کاتالیز نامتقارن شد.
یادداشت
یادداشت 1. این مقاله 1941 سیگار کشیدن در آزمایشگاه (یک عادت به اندازه کافی رایج در روزهای گذشته) را هنگام کار با HCN توصیه می کند، زیرا به دود سیگار طعم خاصی می دهد.
تبصره 2. به جای استفاده از NH4Cl و KCN، ممکن است استفاده از NH کارآمدتر به نظر برسد4CN. افسوس، NH4CN یک جامد پایدار نیست و دارای خاصیت ناگوار انتشار گاز HCN است. راه حل این کار ساختن آن است در موقعیت با NH4Cl و KCN.
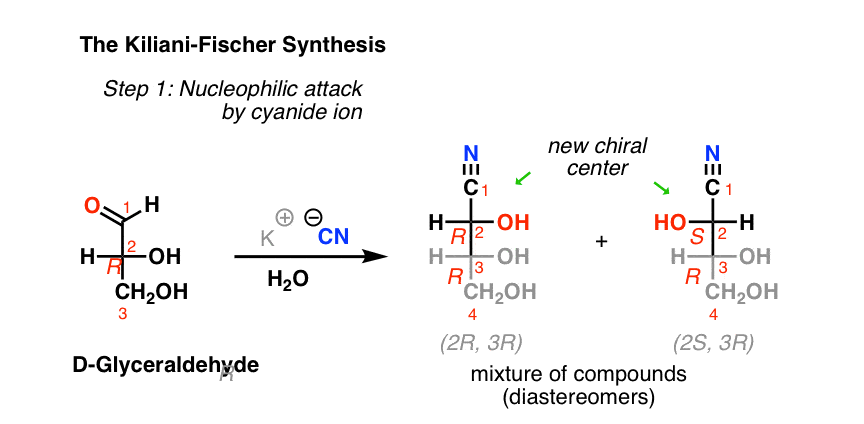
نکته 3. اگر شیمی کربوهیدرات را پوشش داده باشید، ممکن است تشخیص دهید که Strecker پسر عموی نزدیک روش Kiliani-Fischer برای گسترش زنجیره قندها است. همین فکر است!
نمونه های زندگی واقعی
مثال های زندگی واقعی:
سازمان مصنوعی. 1942، 22، 23
لینک DOI: 10.15227/orgsyn.022.0023
سازمان مصنوعی. 1944، 24، 9
لینک DOI: 10.15227/orgsyn.024.0009
سازمان مصنوعی. 1953، 33، 7
لینک DOI: 10.15227/orgsyn.033.0007
(پیشرفته) مراجع و مطالعه بیشتر
این یک واکنش بسیار ساده اما قدرتمند است که شامل سه جزء است: آلدهید/کتون، سیانید و آمین. این محصول یک a-aminonitrile است که می تواند به اسیدهای آمینه هیدرولیز شود.
- Ueber die künstliche Bildung der Milchsäure und einen neuen, dem Glycocoll homologen Körper
آدولف استرکر
فقط لیب ان شیمی. 1850، 75 (1)، 27-45
DOI: 10.1002/jlac.18500750103
من فکر این مقاله اصلی در مورد واکنش استرکر است (متاسفانه من نمی توانم آلمانی بخوانم). اما بیش از 150 سال قدمت دارد، که نشان می دهد این واکنش واقعا ساده و قوی است. - dl-ALANINE
سی کندال و بی اف مک کنزی
سازمان مصنوعی. 1929، 9، 4
DOI: 10.15227/orgsyn.009.0004
یک روش قدیمی اما قابل تکرار برای آلانین راسمیک از طریق سنتز Strecker. - افزودن کاتالیزوری انانتیو انتخابی HCN به کتوئیمین ها. سنتز کاتالیزوری اسیدهای آمینه چهارتایی
پتر واچال و اریک ان. یاکوبسن
نامه های ارگانیک 2000، 2 (6)، 867-870
DOI: 10.1021/ol005636+
واکنش استرکر نامتقارن توجه داشته باشید که این از HCN به عنوان منبع سیانید استفاده می کند، که خوشبختانه به صورت خالص یا گاز استفاده نمی شود، اما قبل از واکنش از TMSCN + متانول در محلول تولید می شود (به یادداشت 10 مراجعه کنید).
