تیونیل کلرید، SOCl2 – واکنش با کربوکسیلیک اسیدها برای دادن هالیدهای اسیدی
- تیونیل کلرید (SOCl2) یک معرف مفید برای تبدیل اسیدهای کربوکسیلیک به کلریدهای اسیدی است.
- همچنین می توان از آن برای تبدیل الکل ها به آلکیل هالید استفاده کرد که در این پست توضیح داده شده است (مقاله: SOCl2 و PBr3 – همچنین خوب است که از S آگاه باشیدنمکانیسم i – SOCl2 و Sنمکانیسم من)
- هالیدهای اسیدی را می توان به تعداد زیادی از گروه های عاملی دیگر (استرها، آمیدها، انیدریدها و همچنین آلدهیدها و کتون ها) از طریق جایگزینی آسیل هسته دوست تبدیل کرد، بنابراین این معرف در سنتز بسیار مفید است.
- معرف های دیگری که همان تبدیل را انجام می دهند PCl هستند3، PCl5، اگزالیل کلرید و معرف های برم مربوطه.
فهرست مطالب
-
- تیونیل کلرید (SOCl2) – ساختار لوئیس
- تبدیل اسیدهای کربوکسیلیک به هالیدهای اسیدی
- تبدیل اسیدهای کربوکسیلیک به هالیدهای اسیدی توسط SOCl2 – سازوکار
- هالیدهای اسیدی در سنتز
- برنامه های کاربردی – برخی از مشکلات سنتز
- خلاصه
- یادداشت
- خودت امتحان کن
- (پیشرفته) مراجع و مطالعه بیشتر
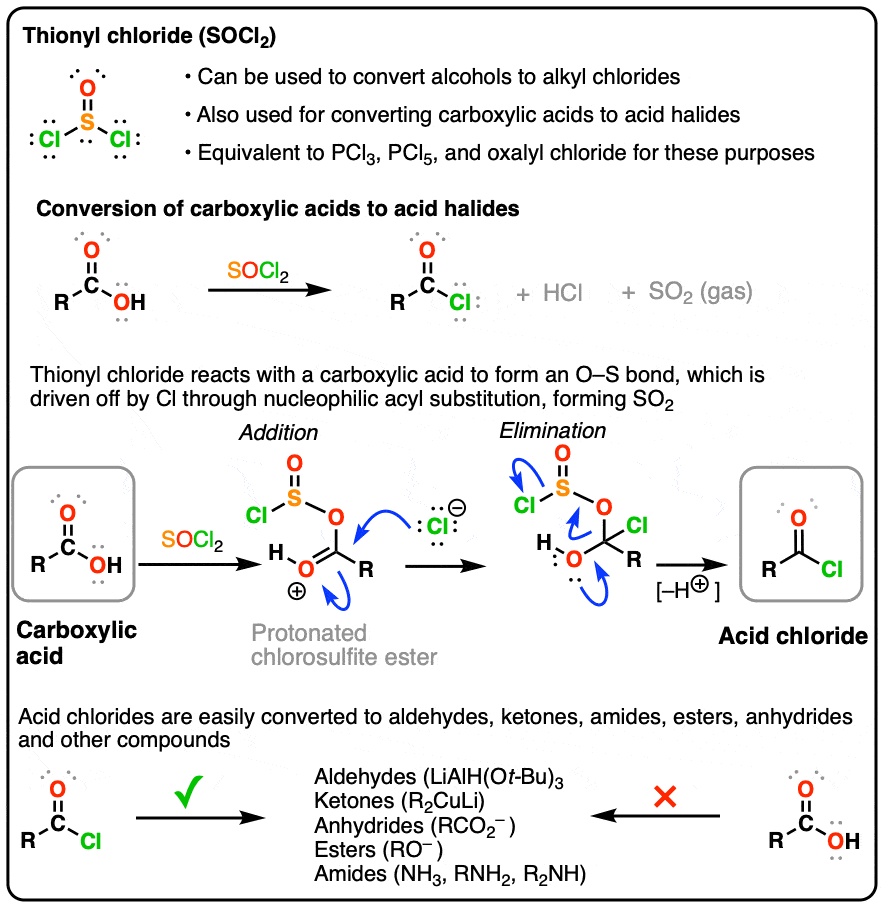
1. ساختار لوئیس تیونیل کلرید (SOCl2)
تیونیل کلرید (SOCl2) یک معرف مفید برای تبدیل الکل ها به آلکیل هالیدها و برای تبدیل اسیدهای کربوکسیلیک به کلریدهای اسیدی است. ما قبلاً در فصل الکل ها با آن آشنا شده ایم. (به مقاله – SOCl مراجعه کنید2 و PBr3)
SOCl2 بوی شیرین و مریضی دارد، مانند تخم مرغ های فاسدی که در شیرین کننده ریخته شده اند: یک بار تجربه شده، هرگز فراموش نمی شوند. اگر تا به حال لذت (غیر) راه رفتن در کنار کارخانه خمیر کاغذ و کاغذ را داشته اید، بسیار شبیه بوی دی اکسید گوگرد است.
هندسه تیونیل کلرید جالب است. در واقع ده (10) الکترون ظرفیت روی تیونیل کلرید وجود دارد، و هندسه ای را اتخاذ می کند که در آن یکی از جفت های تنها یک اوربیتال را اشغال می کند. با سه اتم متصل و یک جفت تنها، این منجر به آرایش چهار وجهی اوربیتال ها و یک هندسه مولکولی هرمی مثلثی (شبیه به NH) می شود.3).
در این مقاله ما عمدتاً در مورد استفاده از تیونیل کلرید در تبدیل اسیدهای کربوکسیلیک به کلریدهای اسیدی صحبت خواهیم کرد، ویژگی که با چندین معرف دیگر مانند تری کلرید فسفر (PCl) مشترک است.3، پنتاکلرید فسفر (PCl5و اگزالیل کلرید.
ما همچنین برخی از کاربردهای تیونیل کلرید را در مسائل سنتز نشان خواهیم داد.
(تیونیل کلرید (SOCl2) گاهی با اشتباه گرفته می شود سولفوریل کلرید (SO2Cl2) سولفوریل کلرید بسیاری از واکنش های مشابه کلر عنصری را انجام می دهد (Cl2) در حالی که برای رسیدگی راحت تر است.)
2. تبدیل اسیدهای کربوکسیلیک به کلریدهای اسیدی
تیونیل کلرید اسیدهای کربوکسیلیک را به کلریدهای اسیدی (“کلریدهای آسیل”) تبدیل می کند. در اینجا یک مثال کلی به همراه چند مثال خاص آورده شده است.
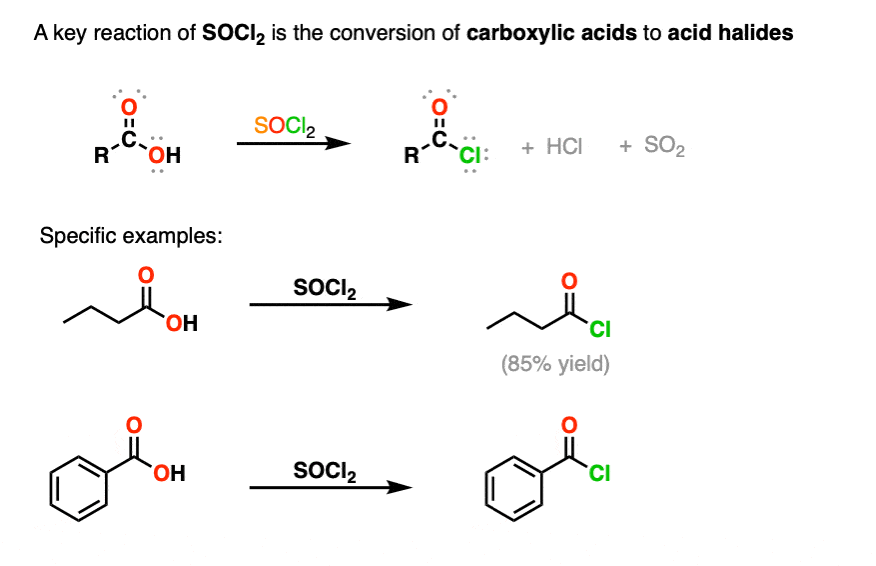
این واکنش همچنین با واکنشگرهای مرتبط PCl کار می کند3، PCl5و اگزالیل کلرید، که برای اهداف ما معادل در نظر گرفته می شوند.
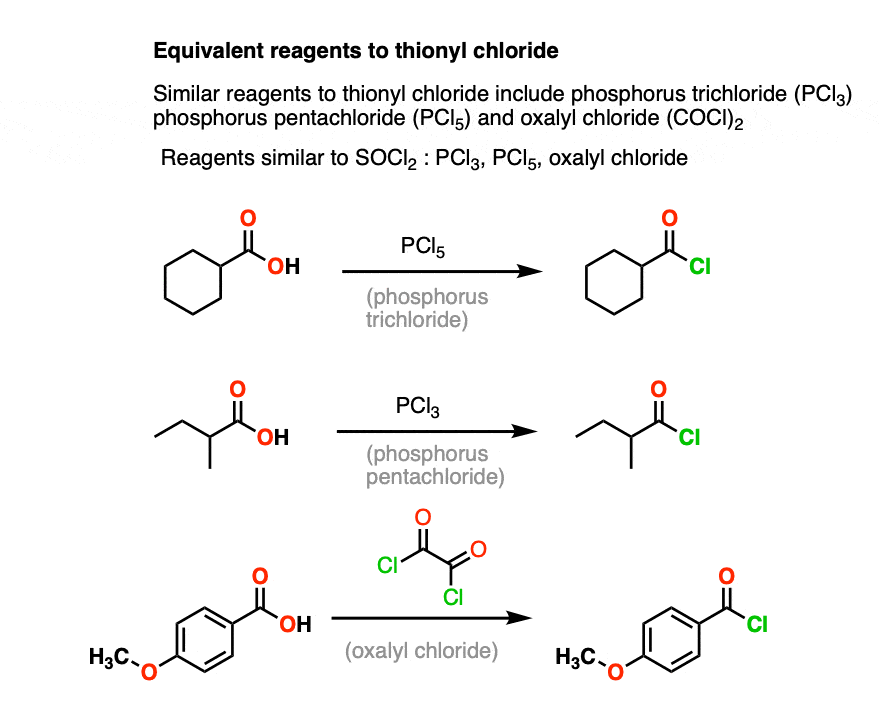
این یک واکنش مفید است زیرا گروه ترک ضعیف HO(-) را به گروه خروجی خوب Cl(-) تبدیل می کند، که باعث می شود گروه کربونیل بسیار بیشتر تحت واکنش های جایگزینی آسیل نوکلئوفیل قرار گیرد. (پست: جایگزینی آسیل نوکلئوفیلیک تحت شرایط اولیه را ببینید)
برای کاربردهای خاص، بخش 4 را در زیر ببینید.
پس چگونه کار می کند؟
3. کربوکسیلیک اسیدها به اسید کلرید با SOCl2 – مکانیسم
تیونیل کلرید با اسیدهای کربوکسیلیک واکنش می دهد و یک هالید اسید، دی اکسید گوگرد (SO2) و HCl.
واکنش اولیه بین اسید کربوکسیلیک (به عنوان یک نوکلئوفیل) است که به اتم گوگرد (الکتروفیل) حمله می کند و در نتیجه H با SO جایگزین می شود.2Cl. [Note 1 – this is called a “chlorosulfite ester”]
نکته کلیدی مرحله اول نشان دادن آن است کربونیل اکسیژن به عنوان هسته دوست عمل می کند! (چرا OH نه؟ دیدن آزمون 1)
از دست دادن کلر از گوگرد را می توان به دو صورت مختلف نشان داد.
- یکی از راههای نشان دادن وقوع این واکنش از طریق واکنش افزودن-حذف در گوگرد است، با این تفاوت که پیوند SO (pi) شکسته میشود (افزودن) و سپس دوباره تشکیل میشود (حذف) و کلر (-) را به عنوان گروه ترک خارج میکند. [Note 2 – not much double bond character in S-O (pi).]
برای دیدن این مکانیسم، ماوس را اینجا نگه دارید یا روی این پیوند کلیک کنید.
- راه دیگری برای نشان دادن آن (در زیر) جابجایی مستقیم در گوگرد است که در نهایت چهار وجهی است. از این نظر میتوانیم این واکنش را بسیار شبیه یک S در نظر بگیریمن2 واکنش در گوگرد.
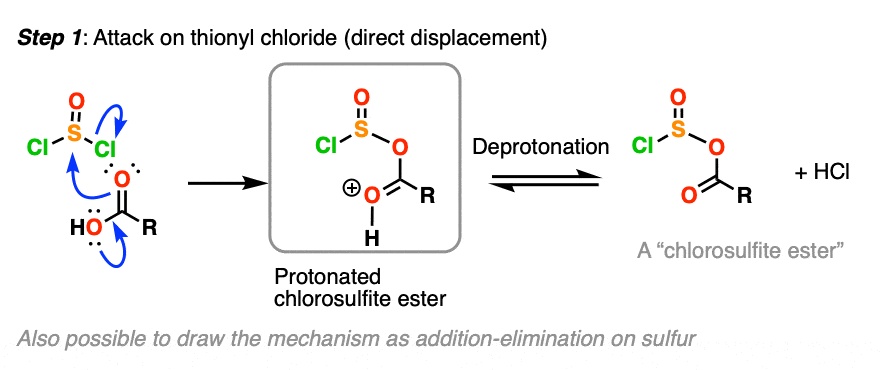
هنگامی که استر کلروسولفیت تشکیل می شود، کلرید اسید از طریق یک مکانیسم کلاسیک حذف-افزودن تشکیل می شود.
- سپس یون کلرید به کربن کربونیل حمله می کند که منجر به تشکیل C-Cl، شکستن CO (pi) می شود.
- پیوند CO pi دوباره تشکیل می شود و پیوند CO شکسته می شود.
سپس کلرید اسید (پروتون دار) حاصل توسط Cl(-) پروتونه می شود تا کلرید اسید بدست آید.
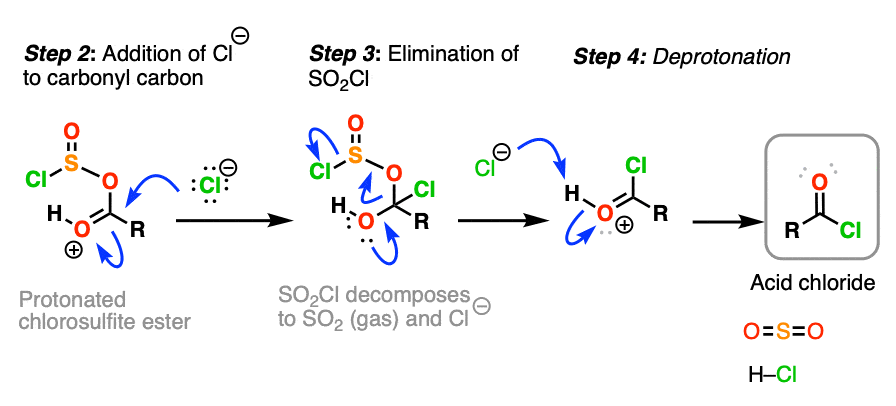
در همین حال، (-)O-SOCl تجزیه می شود و دی اکسید گوگرد بدبو (SO) ایجاد می کند.2) که به صورت گاز حباب می زند و واکنش را برگشت ناپذیر می کند. (واکنشهای مربوط به تیونیل کلرید باید همیشه در هود بخار با تهویه مناسب انجام شود. نکته 3).
4. هالیدهای اسیدی در سنتز
خیلی خوب. بنابراین کربوکسیلیک اسیدها را می توان به هالیدهای اسیدی تبدیل کرد. حالا چی؟
خوب، مجموعه جدیدی از احتمالات را باز می کند. اسیل هالیدها خیلی راحت تر از اسیدهای کربوکسیلیک تحت جایگزینی آسیل نوکلئوفیل می شوند.
اگر کربوکسیلیک اسیدها با آمین ها، آلکوکسیدها یا کربوکسیلات ها (از جمله دیگر) درمان شوند، تنها محصولی که تشکیل می شود یک اسید کربوکسیلیک deprotonated (کربوکسیلات) است.
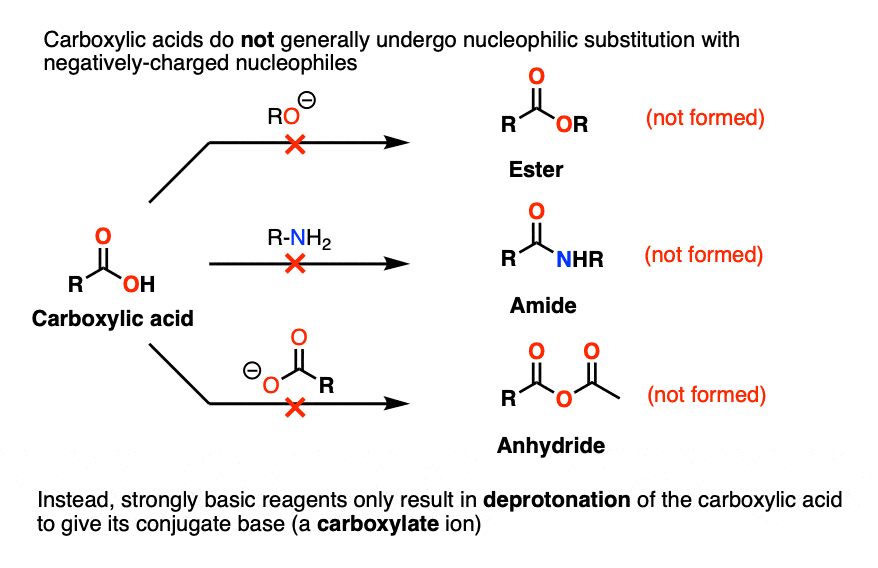
همانطور که قبلاً بحث شد، به این دلیل است که در شرایط بازی، گروه ترک کربوکسیلیک اسید یون هیدروکسید (HO-) نیست، بلکه دی آنیونی (و بسیار بازی) O(2-).
اسیدهای کربوکسیلیک تحت شرایط اسیدی جایگزین آسیل نوکلئوفیل می شوند، اما این داستان متفاوت است. (دیدن مکانیسم های کربونیل – حذف)
با این حال، هنگامی که کربوکسیلیک اسید به هالید اسید تبدیل می شود، تعداد زیادی از واکنش های جایگزینی آسیل نوکلئوفیل ممکن می شود.
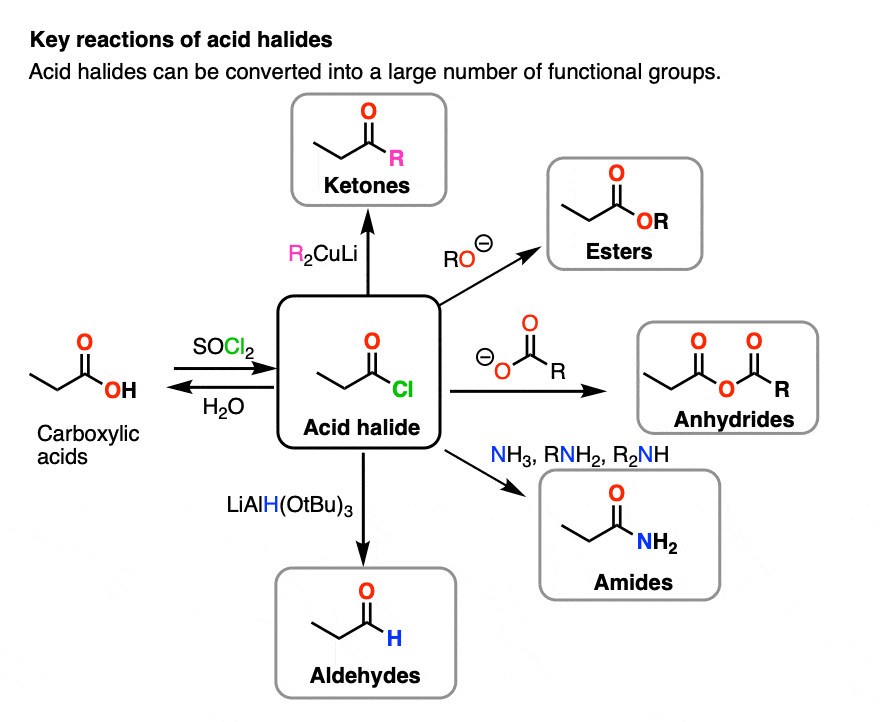
5. برنامه های کاربردی – مسائل سنتز
هنگامی که این واکنش در جعبه ابزار مصنوعی شما قرار می گیرد، راه حل هایی را برای طیف گسترده ای از راه حل ها برای مشکلات سنتز باز می کند.
ببینید آیا می توانید مسیرهای دو مرحله ای برای سنتز هر یک از سه مولکول زیر ایجاد کنید یا خیر.
روشی که در آن SOCl2 تبدیل کربوکسیلیک اسیدها به هالیدهای اسیدی بسیار متنوع تر را امکان پذیر می کند، بسیار شبیه به نحوه تبدیل الکل ها به آلکیل هالیدهای SOCl2 است که می تواند متعاقباً از طریق SN1/SN2/E1/E2 به طیف وسیعی از محصولات مختلف تبدیل شود. واکنش ها (به عنوان مثال، قدرت واکنش SN2 را ببینید)
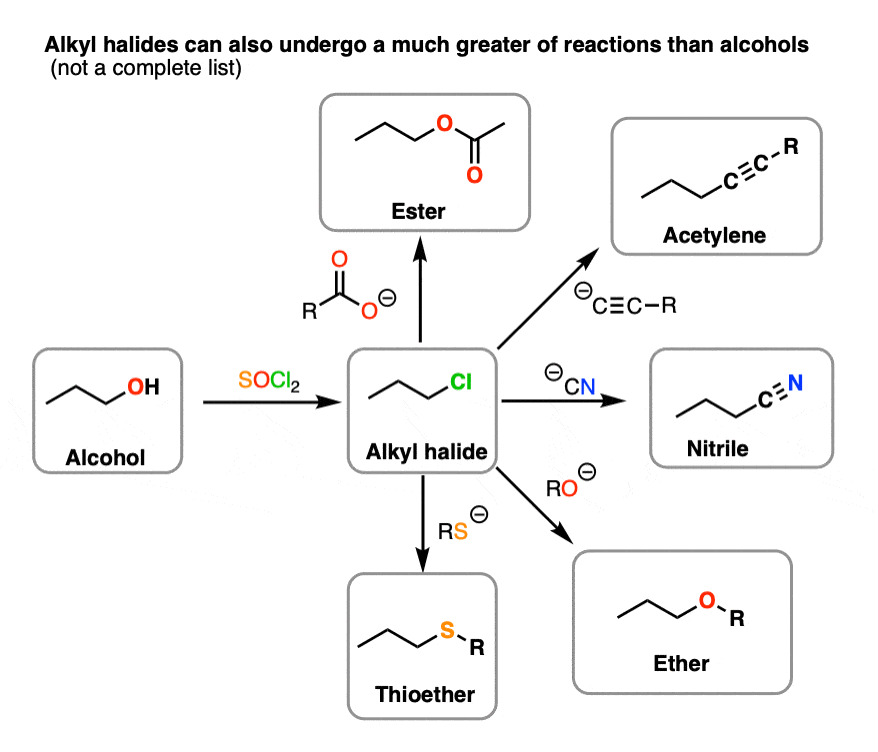
6. خلاصه
- تیونیل کلرید می تواند کربوکسیلیک اسیدها را به اسید هالید تبدیل کند.
- سپس هالیدهای اسید را می توان به آلدئیدها، کتونها، انیدریدها، استرها، آمیدها یا تعدادی از گروههای عاملی دیگر تبدیل کرد. (از جمله بازگشت به اسید کربوکسیلیک – فقط آب اضافه کنید! )
- به این ترتیب، کربوکسیلیک اسیدها را می توان (در حدود 2 مرحله) به انواع زیادی از ترکیبات کربونیل مختلف تبدیل کرد.
- شما باید این واکنش را بدانید (یا موارد دیگر مانند آن، یعنی PCl3، PCl5، اگزالیل کلرید) اگر می خواهید با موفقیت سنتز مشتقات کربوکسیلیک اسید را برنامه ریزی کنید.
یادداشت
یادداشت 1. این اثر جایگزینی OH با گروه خروجی خوب (-)OSOCl است که پایه مزدوج مولکول (ناپایدار) اسید کلروسولفینیک است. به محض اینکه (-)OSOCl جابجا شد، تقریباً بلافاصله به دی اکسید گوگرد (SO) تجزیه می شود.2) گاز و یون کلرید.
تبصره 2. بسیار وسوسه انگیز است که پیوند S=O را بسیار شبیه پیوند C=O بدانیم و مسیرهای واکنش مشابهی مانند حذف-افزودن را طی کند.
با این حال، همبستگی بین C=O و S=O چندان عالی نیست. همانطور که قبلا ذکر شد، اتم گوگرد چهار وجهی است، نه مسطح مثلثی. “مجازات” پرانرژی برای از دست دادن یک گروه ترک در یک sp2 اتم هیبرید شده برای گوگرد سنگین تر و قطبش پذیرتر به طور قابل توجهی کمتر از کربن است. علاوه بر این، SO “پیوند” دارای ویژگی پیوند دوگانه چندانی نیست. اغلب به صورت S(+)-O(-) نوشته می شود تا ماهیت بسیار قطبی این پیوند را منعکس کند.
بنابراین اگرچه ممکن است این مکانیسم نوشته شده را مشاهده کنید، اما این یک سوال باز است که چقدر با واقعیت مطابقت دارد.
نکته 3. یک حادثه که در زمان من به عنوان یک TA رخ داد، شامل پرتاب یک فلاسک با 5 میلی لیتر تیونیل کلرید توسط دانش آموزی در حمام روتوف در خارج از هود بود. ابر SO2 و HCl که تشکیل شد، آزمایشگاه آموزشی را به مدت نیم ساعت پاک کرد، بنابراین می توانید تصور کنید که تیونیل کلرید اگر در معرض رطوبت در ریه های شما قرار گیرد چه کاری انجام می دهد. با احتیاط رفتار کنید، درست همانطور که اگر با فسژن کار می کردید.
خودت امتحان کن
(پیشرفته) مراجع و مطالعه بیشتر
- فتالیل کلراید
P. Kyrides
مجله انجمن شیمی آمریکا 1937، 59 (1)، 206-208
DOI: 10.1021/ja01280a051
مقاله اولیه در مورد تبدیل انیدرید فتالیک به دی اسید با SOCl2، به همان خوبی معکوس واکنش، که می تواند SOCl را بازسازی کند2. - ساختار سوکسینیل دی کلراید و برخی دیگر از ترکیبات دارای عملکرد چرخه ای بالقوه
جیمز کیسون و المر جی ریست
مجله شیمی آلی 1958، 23 (10)، 1492-1496
DOI:10.1021/jo01104a024
در این مقاله، سوکسینیل دی کلرید تنها از اسید با مقدار اضافی SOCl به دست می آید2 و مقدار کاتالیزوری پیریدین. از پیریدین می توان برای کاتالیز واکنش SOCl استفاده کرد2 با اسیدهای کربوکسیلیک - Eine Methode zur katalysierten Herstellung von Carbonsäure- und Sulfosäure-chloriden mit Thionylchlorid
H. Bosshard R. Mory M. Schmid Hch. زولینگر
Helv. چیم. Acta 1959، 42 (5)، 1653-1658
DOI: 10.1002/hlca.19590420526
این مقاله چگونگی DMF (N، N-دی متیل فرمامید، یک حلال رایج) می تواند برای کاتالیز واکنش SOCl استفاده شود.2 با اسیدهای کربوکسیلیک که امروزه معمولاً استفاده می شود. - n– بوتیریل کلرید
Helferich و W. Schaefer
سازمان مصنوعی. 1929، 9، 32
DOI: 10.15227/orgsyn.009.0032
یک روش کلاسیک برای تبدیل اسیدهای کربوکسیلیک به کلرید اسید با SOCl2 از جانب ارگانیک. آلی سنتز، یک منبع قابل اعتماد از تبدیلات آلی به طور مستقل آزمایش شده است.
