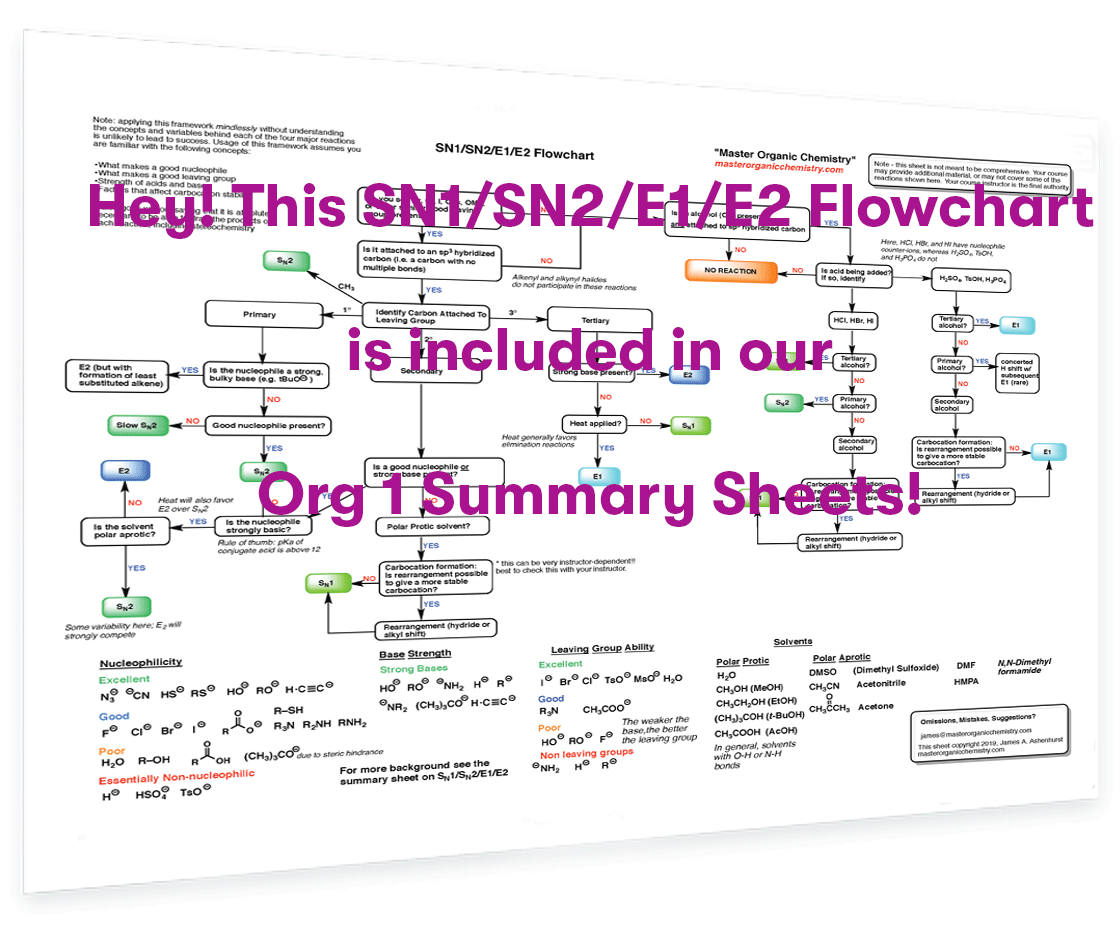
راهنمای سریع N’ Dirty برای واکنشهای SN1/SN2/E1/E2، قسمت 3: نقش حلال
بیایید با راهنمای Quick N Dirty خود در مورد SN1/SN2/E1/E2 ادامه دهیم – یک مرور سریع از تفکر درباره این تصمیم واکنش.
پس از بررسی سوبسترا و باز/هسته دوست در واکنش SN1/SN2/E1/E2، این پست در مورد سوال بعدی است:
حلال چیست؟
به یاد داشته باشید که دو نوع حلال مهم وجود دارد که باید در نظر بگیرید: پروتیک قطبی حلال ها و آپروتیک قطبی حلال ها [See: All About Solvents]
بیایید یک بررسی کوچک انجام دهیم و ابتدا حلال های قطبی پروتیک را بررسی کنیم.
حلال های پروتیک قطبی قادر به پیوند هیدروژنی هستند. به یاد بیاورید که پیوند هیدروژنی در جایی اتفاق می افتد که ما یک اتم بسیار الکترونگاتیو مانند O یا N داشته باشیم که مستقیماً به هیدروژن پیوند خورده باشد:
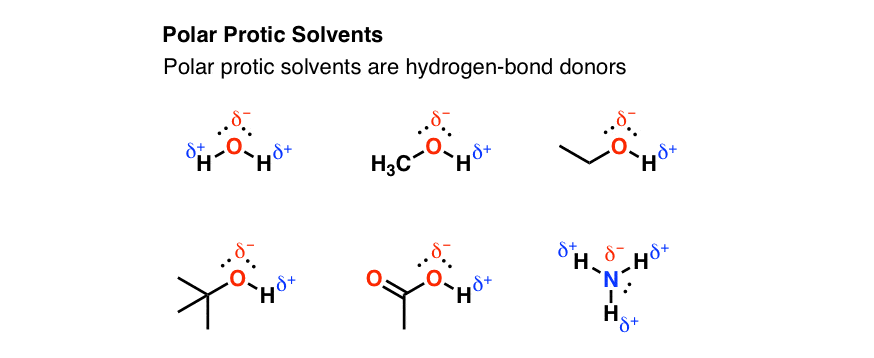
نکته کثیف Quick N’: حلال های دارای گروه های OH یا NH قطبی هستند پروتیک حلال ها
پیوند هیدروژنی مستقیماً مسئول نقاط جوش بالای حلالهایی مانند آب و اتانول است. بارهای مثبت جزئی هیدروژن به بارهای منفی جزئی اتم های الکترونگاتیو جذب می شوند. همچنین به همین دلیل است که آب حلال بسیار خوبی برای گونه های باردار مانند یون های هالید است. حلال های پیوند هیدروژنی یون های دارای بار منفی را مانند یک ژاکت احاطه کرده اند.

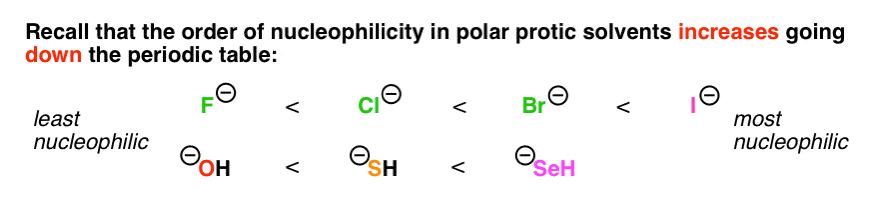
حلال های قطبی پروتیک از طریق پیوند هیدروژنی به هسته دوست ها می چسبند و با پایین آمدن جدول تناوبی، هسته دوستی افزایش می یابد.
این «جلیقه» از مولکولهای حلال – بسیار شبیه به انبوهی از بابیها – به این معنی است که این آنیونها آزادی عمل را ندارند که اگر توسط انبوهی از مولکولهای حلال احاطه نشده بودند، معمولاً داشتند. یعنی نوکلئوفیل ها کمتر هسته دوست می شوند! تمایل به تشکیل پیوندهای هیدروژنی برای یونهای کوچک و بسیار الکترونگاتیو مانند فلوئور بالاترین است و با بزرگتر شدن یونها (و بار پراکنده تر) کاهش می یابد.
این بدان معنی است که در پروتیک قطبی حلال ها، هسته دوستی آنیون های هالید افزایش همانطور که ما می رویم پایین جدول تناوبی
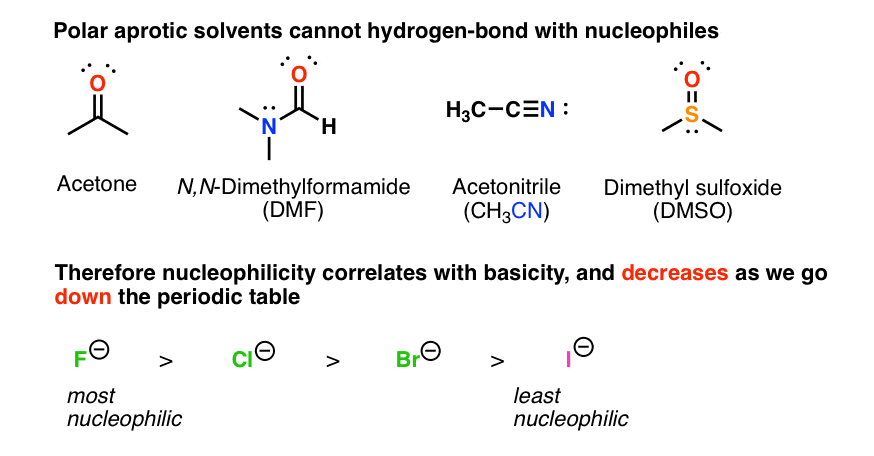
قطبی آحلال های پروتیک با هسته دوست ها پیوند هیدروژنی ندارند و بنابراین هسته دوستی در این حلال ها با پایه همبستگی دارد.
حالا بیایید در مورد حلال های آپروتیک قطبی صحبت کنیم. حلال های آپروتیک قطبی به اندازه کافی قطبی هستند که گونه های باردار (مانند یون های هالید) را حل کنند، اما پیوند هیدروژنی را اهدا نمی کنند. این بدان معناست که در حلالهایی مانند DMSO، DMF، استون، یا استونیتریل، هسته دوستی با باز بودن (و استحکام پیوند، مانند CF > C-Cl > C-Br > CI) – و در نتیجه هسته دوستی بسیار بهتر همبستگی دارد. کاهش می دهد همانطور که جدول تناوبی را پایین می آوریم.
بنابراین وقتی صحبت از SN1/SN2/E1/E2 به میان میآید، نتیجه نهایی چیست؟
نتیجه نهایی این است:
- Quick N’ Dirty قانون شماره 5: قطبی پروتیک حلال ها تمایل دارند حذف (E2) به پایان رسید جایگزینی (SN2). پخورشیدی غیر طبیعی حلال ها تمایل به جایگزینی (SN2) نسبت به حذف (E2) دارند.
بیایید به نمونه هایی که در دو پست اول بررسی کردیم برگردیم.
عملا، شما فقط باید حلال را در تصمیم SN1/SN2/E1/E2 در نظر بگیرید که قبلاً بستر و هسته دوست/پایه را تجزیه و تحلیل کرده باشید.
این معمولاً زمانی اتفاق میافتد که یک آلکیل هالید ثانویه با یک هسته دوست قوی مانند NaOCH دارید.3 یا NaOH
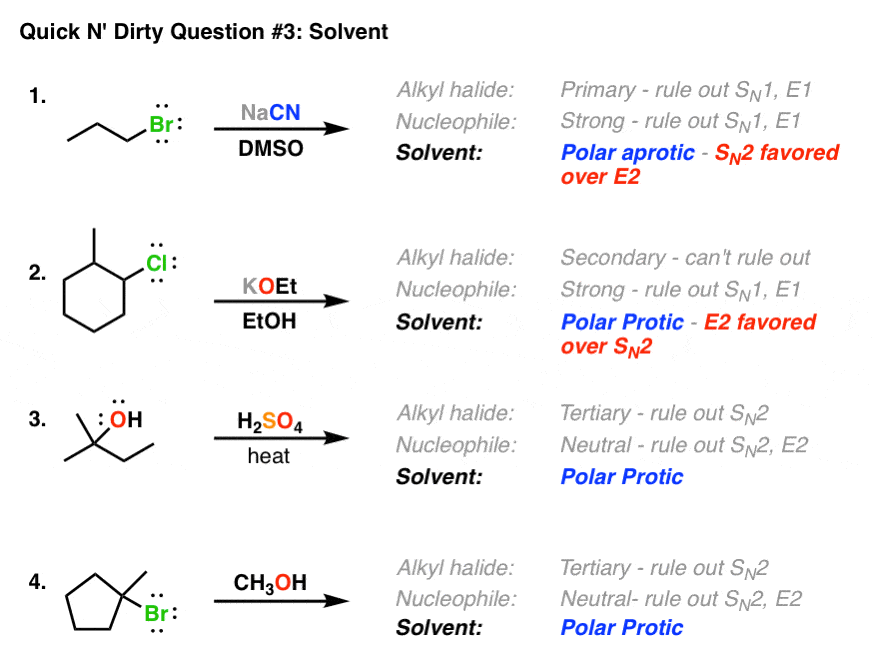
این به ویژه در مثال شماره 2 صادق است، جایی که ما واقعاً نمیتوانیم در مورد SN2 یا E2 صحبت کنیم تا زمانی که حلال را بررسی کنیم. این واقعیت که ما از یک حلال پروتیک قطبی (EtOH) استفاده می کنیم، بخش مهمی از اطلاعات است که واکنش را به عنوان E2 نشان می دهد.
در آخرین پست این مجموعه به تاثیر دما بر این واکنش ها خواهیم پرداخت.
[Edit Dec 13]: نقطه ضعف رویکرد Quick N’ Dirty چیست؟ خوب، واقعاً وضعیت واقعی را در این واکنش ها نشان نمی دهد، یعنی همیشه یک محصول را منحصرا نمی دهند. بنابراین به خاطر داشته باشید که وقتی رویکرد Quick N’ Dirty می گوید که E2 محصول اصلی است، ممکن است مقدار کمی SN2 رقیب نیز وجود داشته باشد، یا اگر SN1 مورد علاقه باشد، ممکن است مقادیر کمی از محصولات واکنش دیگر نیز داشته باشید. . نکات کلیدی این تمرین این است که 1) عوامل اصلی مؤثر بر هر نوع واکنش را به خاطر بسپارید و 2) هنگامی که نوع واکنش را شناختید، بتوانید آن را اعمال کنید.
آیا با SN1/SN2/E1/E2 مبارزه می کنید؟ برگههای خلاصه Org 1 ما (PDF) حاوی یک فلوچارت تمام صفحه در مورد تصمیمگیری SN1/SN2/E1/E2، و همچنین دو صفحه دیگر که خلاصهای از واکنشهای جایگزینی و حذفی، علاوه بر بسیاری از موضوعات دیگر Org 1 است.