برم سازی آلکن ها: مکانیسم
برم سازی آلکن ها چگونه کار می کند؟
در پست قبلی نشان دادیم که چگونه مکانیسم برماسیون آلکنها نمیتواند از یک واسطه کربوکاتیونی عبور کند.
چرا که نه؟ ما حداقل 3 دلیل خوب داریم:
- این استریو انتخابی است. دو اتم که پیوندهای جدیدی با کربن تشکیل می دهند به آن اضافه می شوند وجوه مخالف آلکن (ضد انتخابی استری)
- واکنش این است استریو خاص – (Z)-2-butene محصول(های) متفاوتی نسبت به (E)-2-butene می دهد (در واقع محصولات استریو ایزومرهای یکدیگر هستند).
- بدون تنظیم مجدد مشاهده میشوند، مثلاً برای واکنشهای H-Cl با آلکنهای خاص
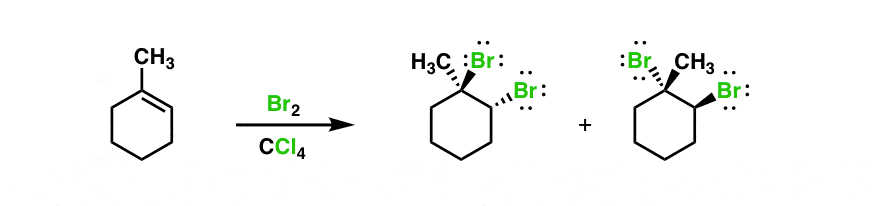
هیچ یک از این نتایج با واکنشی که از طریق یک کربوکاتیون مسطح می گذرد سازگار نیست.
یک جزئیات دیگر برای توضیح وجود دارد: هنگام استفاده از آب به عنوان یک حلال، واکنش با انتخاب منطقه ای “مارکونیکوف” ادامه می یابد. یعنی پیوند CO بر روی جایگزین ترین کربن آلکن تشکیل می شود.
فهرست مطالب
- برماسیون از طریق یک ماده میانی 3 عضوی “یون برومینیم” انجام می شود
- هنگامی که آب یا الکل ها حلال هستند، انتخاب منطقه ای “Marknovnikov” مشاهده می شود
- مکانیسمهای واکنش هرگز نمیتوانند «اثبات» شوند، اما…
- یادداشت
- (پیشرفته) مراجع و مطالعه بیشتر
1. مکانیسم برماسیون از طریق یک ماده میانی 3 عضوی “یون برومینیم” انجام می شود.
در سال 1937، رابرتز و کیمبال از مشاهدات مشابهی استفاده کردند تا به کمبود مکانیسم کربوکاتاسیون آزاد که قبلا توسط رابینسون پیشنهاد شده بود اشاره کنند. [see note]. آنها استدلال کردند که کربوکاتیون آزاد امکان چرخش در اطراف پیوند کربن-کربن را فراهم می کند و این با محصولات مشاهده شده در این واکنش ناسازگار است.
در عوض، آنها واسطه ساختار حلقه 3 عضوی با بار مثبت بر روی هالوژن را فراخوانی کردند که به عنوان عضوی از خانواده اکسیژن “ایزوالکترونیک” است (یعنی همان پیکربندی الکترونیکی را دارد). [epoxides, for instance]. نکته مهم این است که گفتند:
از آنجایی که دو کربن در [the structure] آنها توسط یک پیوند و توسط یک پل هالوژن به هم متصل می شوند، چرخش آزاد قابل انتظار نیست.
علاوه بر این، این پیشنهاد همچنین استریوشیمی واکنش را توضیح می دهد:
این مرحله دوم، که ممکن است افزودن یک یون هالوژن X- یا یک اتم یا مولکول دیگر باشد، احتمالاً یک واکنش ساده “سه اتمی” است… در این حالت اتم جدید از کنار به یکی از اتم های کربن نزدیک می شود. برخلاف اتم X که قبلاً وجود دارد. هنگامی که پیوند X اصلی به کربن با خنثی شدن بار یون به طور همزمان شکسته می شود، پیوندی با این کربن ایجاد می شود. این روند همیشه منجر به ترانس علاوه بر این
موضوع نهایی – چیزی که ما اکنون آن را می نامیمانتخاب منطقه ای” – به طور خاص در این مقاله به آن پرداخته نشده است، اما زمانی منطقی است که شما در نظر بگیرید که این موضوع است کربنس که در این ساختار الکتروفیل هستند نه برم [despite the positive formal charge on bromine, recall that bromine is more electronegative than carbon!] و واکنش در کربنی که به بهترین وجه قادر به تثبیت بار مثبت است ادامه خواهد یافت.
در اینجا به صورت گرافیکی به نظر می رسد:

بنابراین در این واکنش، آلکن به عنوان یک عمل می کند هسته دوست، حمله به الکتروفیلیک برم که باعث ایجاد یک حلقه میانی 3 عضوی می شود. سپس از پشت مورد حمله قرار می گیرد [similar to the backside attack in the SN2] در کربن بهترین قادر به تثبیت بار مثبت، به محصول ترانس. [Note that, like a flat coin that can land on “heads” or “tails” with equal likelihood, the bromine can “land” on either face of the alkene – this gives rise to enantiomers in this case].
2. هنگامی که آب یا الکل ها حلال هستند، انتخاب منطقه ای “Marknovnikov” در تشکیل بروموهیدرین ها مشاهده می شود.
اگر از حلالی استفاده کنیم که به طور بالقوه می تواند به عنوان یک هسته دوست مانند آب یا الکل عمل کند، یون هالونیوم میانی می تواند توسط حلال “به دام افتاده” شود و در مواردی که حلال آب است، محصولات “هالوهیدرین” تولید می شود. مجدداً توجه داشته باشید که مولکول آب به کربن جایگزین شده حمله می کند:
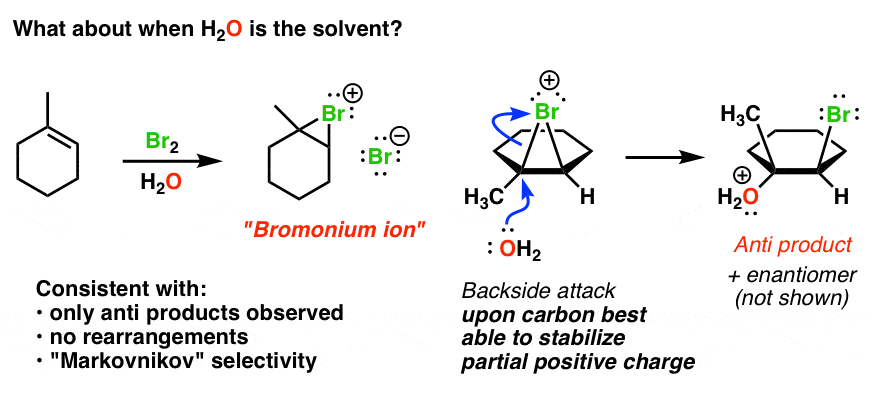
چرا جایگزین ترین کربن؟ زیرا این کربنی است که به بهترین وجه قادر به تثبیت بار مثبت است و از آنجایی که جزئی ترین ویژگی مثبت را دارد، الکتروفیل ترین آن در بین دو کربن نیز خواهد بود.
[Worth noting: bromination of alkenes is technically an oxidation reaction, because each carbon goes from being bound to another carbon (0) to bromine (–1). The oxidation state of each carbon in ethene is +2; the oxidation state of each carbon in dibromoethane is +1. ]
3. مکانیسمهای واکنش هرگز نمیتوانند «اثبات» شوند، اما… مکانیسم برمسازی روی زمین بسیار جامد است.
بسیار خوب – بنابراین به نظر می رسد این پیشنهاد “یون هالونیوم” به اندازه کافی این نتایج را توضیح می دهد. ایده خوبی است. اما آیا وجود دارد شواهد محکم که از سال 1937 آشکار شده است و به ما کمک می کند تا بدانیم آیا آنها هستند یا خیر واقعا وجود دارد؟
در واقع، بله: یون های هالونیوم در واقع در طبیعت مشاهده شده است! یون هالونیوم حاصل از واکنش زیر به ویژه پایدار است. [think about it for a second – why might this be?]
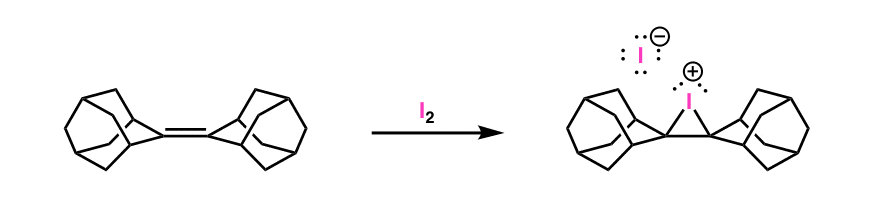
علاوه بر این، RS Brown و همکارانش موفق به استفاده از پراش اشعه ایکس برای به دست آوردن ساختار بلوری این مولکول شدند. در اینجا بخش یون یدونیوم ساختار آمده است:
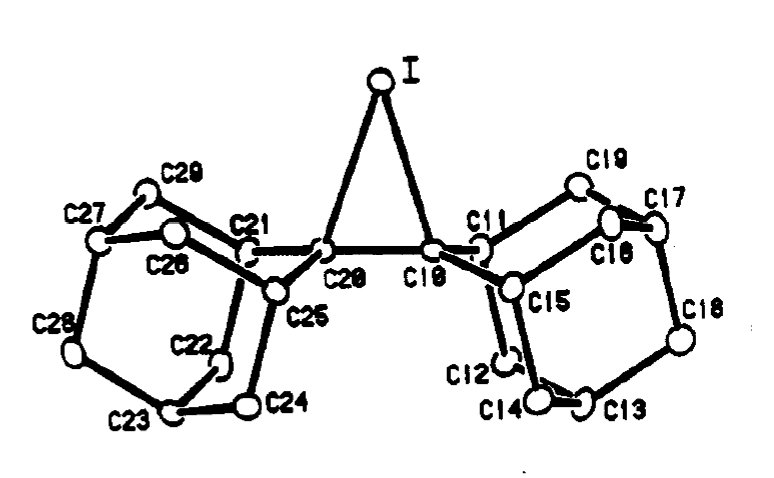
در شیمی، به دست آوردن ساختار بلوری اشعه ایکس از یک مولکول به عنوان “اثبات” تقریباً قطعی وجود آن در نظر گرفته می شود. اگرچه مکانیسم ها هرگز نمی توانند “اثبات” شوند، این ساختار کریستالی تقریباً نزدیک به یک مدرک قطعی است که می توانید بدست آورید.
در پست بعدی این ایده یون های پل میانی را برای توضیح نتایج یک مجموعه کامل از واکنش های دیگر گسترش خواهیم داد.
پست بعدی: الگوی افزودن آلکن شماره 2 – مسیر “حلقه 3 عضوی”
یادداشت
برنده جایزه نوبل 1952 رابینسون، (از شهرت رابینسون Annulation)، مرد باهوشی بود، اما او در مورد مکانیسم این واکنش بر اساس مرجعی که در حال حاضر نمی توانم به دست بیاورم، اما ظاهراً در اینجا به آن اشاره شده، اشتباه کرده است. [Ingold, Chem. Rev., 15, 225, 1934] این آموزنده است: با نگاه کردن به عقب، واضح به نظر می رسد که پیشنهاد هالونیوم درست است، اما در علم ما با نگاه کردن به شیشه جلوی مه آلود به جلو حرکت می کنیم.
ببینید: رابرتز و کیمبال http://pubs.acs.org/doi/abs/10.1021/ja01284a507
(پیشرفته) مراجع و مطالعه بیشتر
- نرخ نسبی برماسیون الفین ها
هارولد اس دیویس
مجله انجمن شیمی آمریکا 1928، 50 (10)، 2769-2780
DOI: 1021/ja01397a031
مقاله اولیه ای که سینتیک بروماسیون آلکن را تحت شرایط مختلف مطالعه می کند. - هالوژناسیون اتیلن ها
ایروینگ رابرتز و جورج ای کیمبال
مجله انجمن شیمی آمریکا 1937، 59 (5)، 947-948
DOI: 1021/ja01284a507
یکی از اولین توصیفات در ادبیات یک یون برومونیوم سه عضوی، که برای ضد استریوشیمی این واکنش - یون های کربنیوم پایدار LXII. تشکیل یون هالونیوم از طریق مشارکت هالوژن مجاور: اتیلن هالونیوم، پروپیلن هالونیوم و یون های 1،2-دی متیل اتیلن هالونیوم
جورج A. Olah، J. Martin Bollinger، و Jean Brinich
مجله انجمن شیمی آمریکا 1968، 90 (10)، 2587-2594
DOI: 1021/ja01012a025
این مقاله اولیه در مورد شناسایی NMR یونهای هالونیوم (کلرونیم 3 عضوی، یدونیوم و برومونیوم) با یونیزاسیون 1،2-دی هالواتانها در محیط سوپراسید (SbF) است.5/بنابراین2). - مسئله تشکیل برگشت پذیر یون های برومونیوم در جریان برم سازی الکتروفیلیک الفین ها. 2. ساختار کریستالی و مولکولی یون برومونیوم آدامانتیلیدین آدامانتان
H. Slebocka-Tilk، RG Ball، و R. Stan Brown
مجله انجمن شیمی آمریکا 1985، 107 (15)، 4504-4508
DOI: 10.1021/ja00301a021
این مقاله ساختار کریستالی اشعه ایکس یک یون برومونیوم ایزوله و پایدار را توصیف می کند. این مهم است زیرا واسطه بودن این یون های برومونیوم حلقوی سه عضوی را در افزودن الکتروفیل برم به آلکن ها ثابت می کند. - یون های برومونیوم و یدونیوم پایدار از الفین های مسدود شده آدامانتیلیدن آدامانتان و بیسیکلو[3.3.1]nonylidenebicyclo[3.3.1]نونان ساختار اشعه ایکس، انتقال هالوژن های مثبت به اولفین های گیرنده و مطالعات اولیه
RS Brown، RW Nagorski، AJ Bennet، RED McClung، GHM Aarts، M. Klobukowski، R. McDonald، و BD Santarsiero
مجله انجمن شیمی آمریکا 1994، 116 (6)، 2448-2456
DOI: 10.1021/ja00085a027
یونهای یدونیوم حلقوی، مشابه یونهای برومونیوم، نیز میتوانند جداسازی و مشخص شوند. آلکن اصلی در این مطالعات، adamantylideneadamantane، با استفاده از واکنش McMurry با 2-adamantanone تهیه می شود. - بررسی مراحل اولیه بروماسیون الکتروفیلیک از طریق مطالعه واکنش با الفین های فضایی انباشته شده
آر اس براون
حساب های تحقیقات شیمیایی 1997، 30 (3)، 131-137
DOI: 10.1021/ar960088e
گزارشی از RS Brown که تحقیقاتی را که او در مورد بازجویی از واسطه های یون برومونیوم با روش های مختلف انجام داد را شرح می دهد. - ALKYNE از طریق فاز جامد مایع – انتقال کاتالیزور دهیدروهالوژناسیون: استیلن دیکاربوکسالدئید تترا متیل استال و استیلن دیکاربوکسالدئید دی متیل استال
Rufine Akué-Gédu و Benoît Rigo
سازمان مصنوعی. 2005، 82، 179
DOI: 10.15227/orgsyn.082.0179 - اصول یک نظریه الکترونیکی واکنش های آلی.
کریستوفر کی اینگولد
بررسی های شیمیایی 1934، 15 (2)، 225-274
DOI: 1021/cr60051a003 - -قدرت های دستوری نسبی گروه هایی از اشکال RO و RR′N در جایگزینی آروماتیک. قسمت چهارم بحث در مورد مشاهدات ثبت شده در بخش های I، II و III
جیمز آلن، آلبرت ادوارد آکسفورد، رابرت رابینسون و جان چارلز اسمیت
جی. شیمی. Soc. (نسبت) 1926، 129، 401-411
DOI: 10.1039/JR9262900401
