باز کردن اپوکسیدها با اسید آبی
در اینجا چیزی است که ما در این پست به آن می پردازیم.
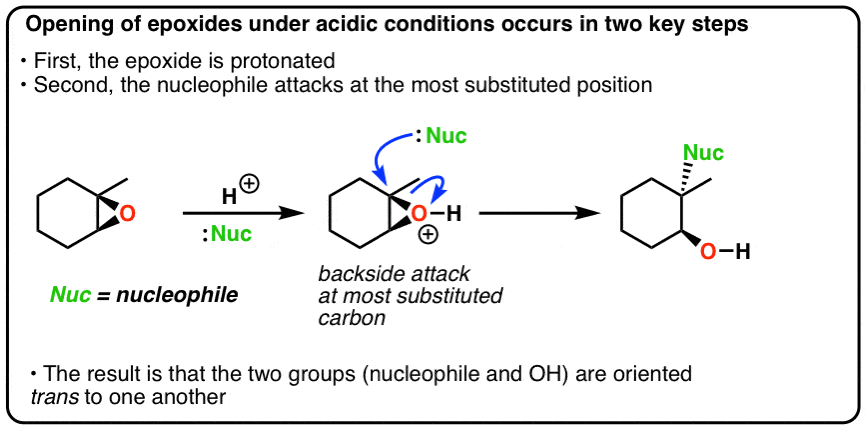
1. تشکیل ترانس-دیول ها از طریق باز شدن اپوکسیدها با اسید آبی
در آخرین پست، نمونه هایی از این که چگونه اپوکسیدها نسبت به اترهای معمولی به طور قابل توجهی نسبت به شکستگی واکنش نشان می دهند را دیدیم. مثلا اسید آبی [often abbreviated “H3O+”] یک اپوکسید را در شرایط بسیار ملایم تری نسبت به یک اتر “معمولی” مانند دی اتیل اتر باز می کند، زیرا اپوکسیدها دارای کرنش حلقه قابل توجهی هستند. [about 13 kcal/mol].
با نگاهی دقیق تر به واکنش، ما همچنین به دو الگوی جالب توجه کردیم:
- حملات هسته دوست در موقعیت “جایگزین تر” اپوکسید (C-1، زیر)
- وارونگی استریوشیمی در این موقعیت اتفاق میافتد، اما نه در موقعیت دیگر (توجه داشته باشید که پیوند CO در C-2 زیر یک “گوه” در ماده اولیه و محصول است).
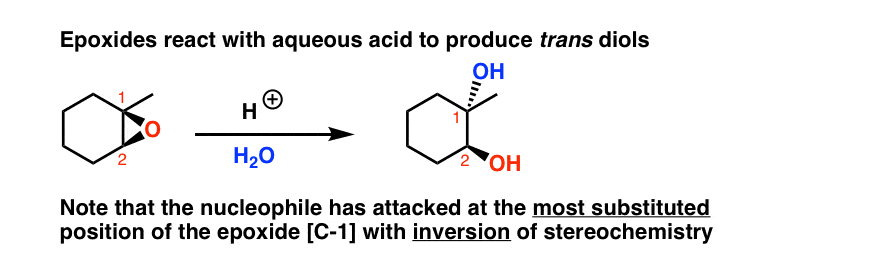
[By the way, how do we “know” that the OH on C-1 is from the nucleophile and is not the epoxide? Using isotopic labels is one way. Another is to use nucleophiles other than water – see below]
لازم به ذکر است که در عدم وجود اسید، هیچ واکنشی رخ نمی دهد. بنابراین واضح است که H+ نقش کلیدی ایفا می کند.
چه اتفاقی می تواند بیفتد؟
در قیاس با واکنش اترها با اسید، اولین مرحله باید واکنش اساسی ترین محل روی مولکول – اپوکسید اکسیژن – با اسید باشد که به ما یک اپوکسید پروتونه می دهد. این به عنوان یک گروه ترک بسیار بهتر از اپوکسید بدون پروتون عمل می کند. [the conjugate acid is always a better leaving group]
سپس مرحله بعدی باید واکنش بهترین هسته دوست موجود در محلول باشد – H2O، در این مورد – با اپوکسید پروتونه ما. و این در جانشین ترین موقعیت، همیشه با وارونگی استریوشیمی رخ می دهد. بنابراین، همانطور که در S مشاهده می کنیم، باید یک “حمله از پشت” به این کربن انجام دهدن2 واکنش پروتون زدایی نهایی محصول خنثی را به ما می دهد.
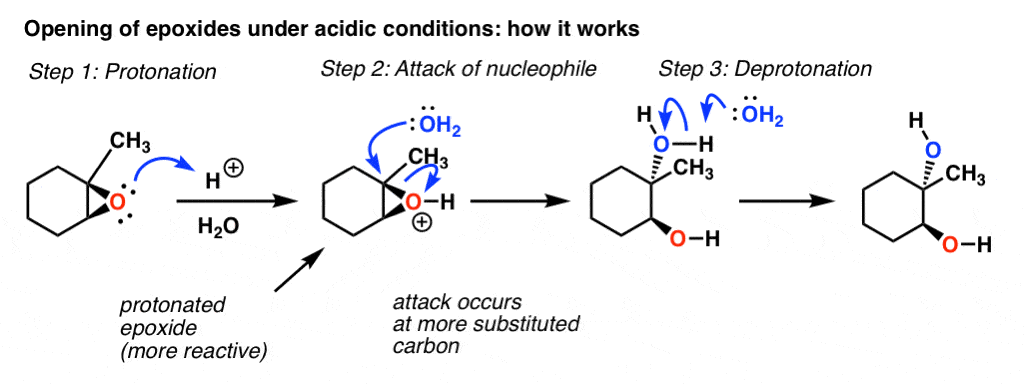
یک ثانیه نگه دارید. اگر درس کلیدی S را به خاطر داریدن2 – اینکه با مانع فضایی ناپسند است – ممکن است عجیب به نظر برسد. اگر این یک S “خالص” بودن2، واکنش، آیا ما انتظار نداریم که حمله به عنوان موقعیت “کمترین جایگزین” رخ دهد؟
واضح است که اینجا باید چیز دیگری در جریان باشد!
2. مکانیسم باز کردن اپوکسیدها با اسید درست مانند باز کردن یون های هالونیوم و جیوه است.
خوشبختانه، احتمالاً قبلاً با چنین واکنش هایی روبرو شده اید! اگر به فصل آلکن ها فکر کنید، ممکن است ببینید که اپوکسید پروتونه شده شباهت عجیبی به دو واسطه واکنشی دیگر دارد که در آن فصل ملاقات کردید: یون های هالونیوم و یون های جیوه، که هر دو حلقه 3 عضوی دارند. بار مثبت:
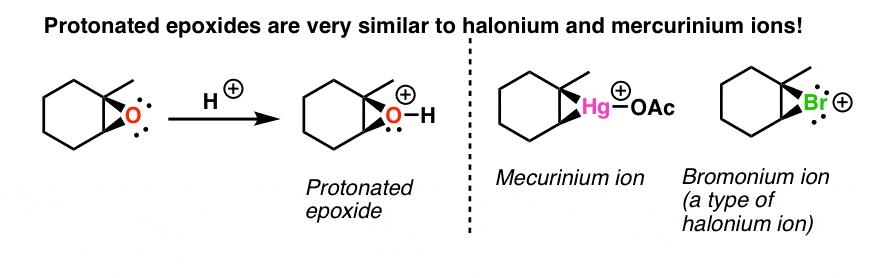
اگر به نحوه واکنش این گونهها با هستهدوستها فکر کنید، همیشه در این مورد بوده است جایگزین تر موقعیت با وارونگی از استریوشیمی در واقع، یک خانواده کامل از واکنشهای افزودن آلکن وجود دارد که این مکانیسم را انجام میدهند که آن را «مسیر حلقهای 3 عضوی» نامیدیم. تشکیل هالوهیدرین یک مثال کامل است:
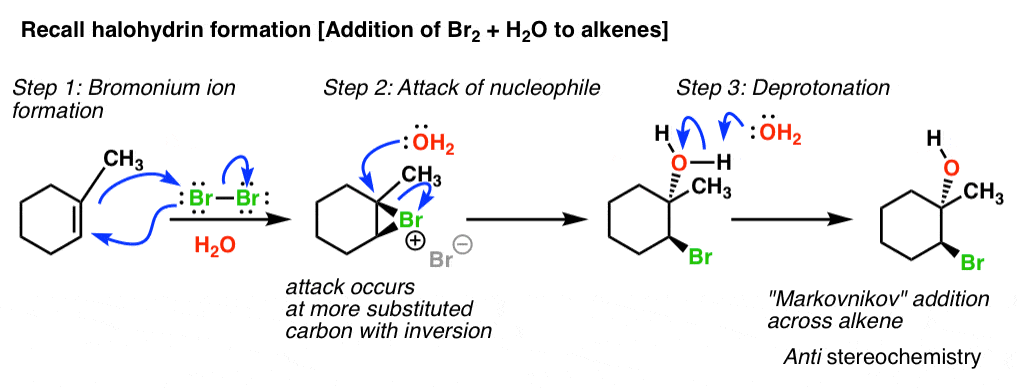
بنابراین در اصل، افزودن نوکلئوفیل ها به اپوکسیدهای پروتونه تنها نمونه دیگری از “مسیر حلقه 3 عضوی” آلکن ها است!
[Need a review on why the nucleophile attacks the most substituted carbon? See this note below and then come back]
اکنون – ما دیدیم که این با اسید آبی کار می کند [H3O+]. آیا می توانیم این را به دیگر هسته دوست ها تعمیم دهیم؟ مطمئن! با چند رزرو که در یک ثانیه به آنها خواهیم رسید.
3. سایر هسته دوست ها چطور؟ الکل ها و HX نیز کار می کنند
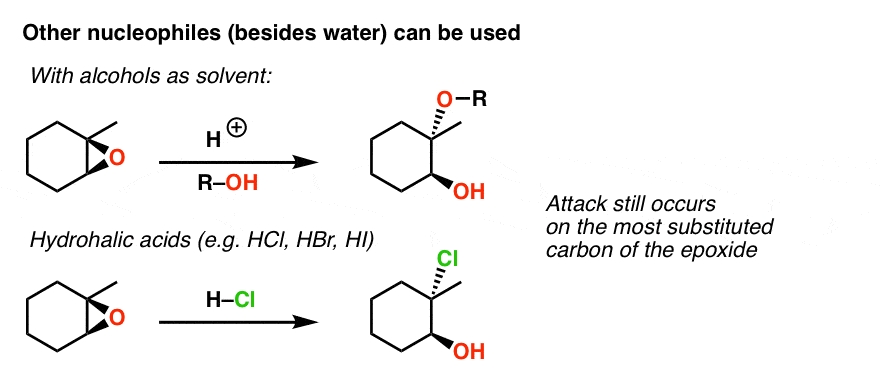
تغییر حلال از آب به الکل منجر به اضافه شدن الکل به جای آن می شود. به عنوان مثال، اگر از CH3OH به عنوان حلال به جای آب استفاده کنیم، محصول ما حاوی OCH خواهد بود3 به جايگزين ترين موقعيت پيوست.
اسیدهای هیدروهالیک [HCl, HBr, and HI] همچنین می تواند به خوبی کار کند و هالوهیدرین ها را تشکیل دهد.
4. چه زمانی نمی کند کمک اسید؟ وقتی نوکلئوفیل با اسید قوی سازگار نیست
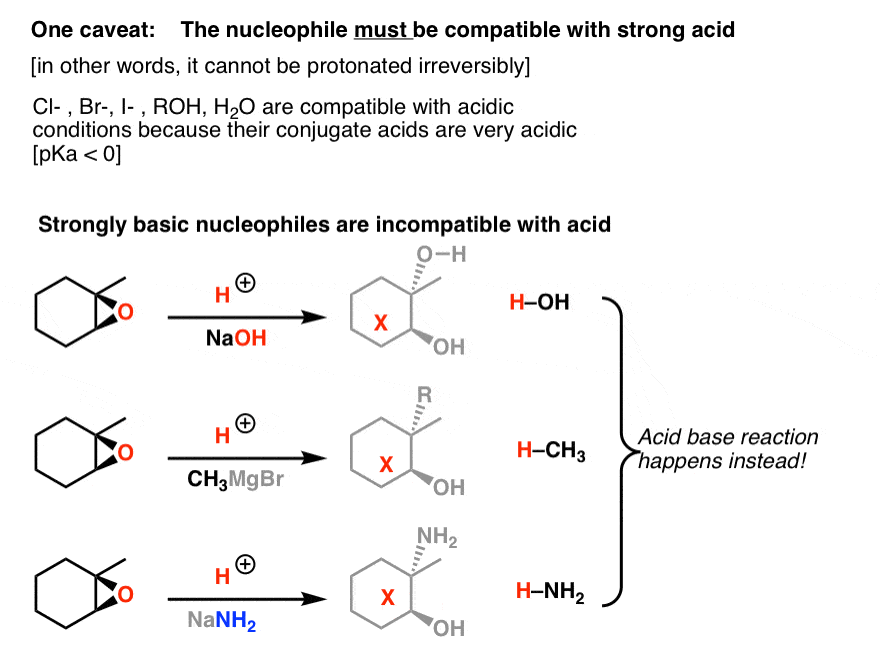
اکنون، ممکن است فکر کنید – اگر اپوکسیدها با استفاده از اسید واکنشپذیرتر شوند، آیا نمیتوانیم این را به دیگر هستهدوستها نیز تعمیم دهیم؟ مثلاً NaOH یا NaNH چطور؟2یا حتی معرف های گریگنارد؟
این معضل نهفته است. شرایط اسیدی فقط با نوکلئوفیل هایی که پروتونه می شوند سازگار است قابل برگشت. [in other words, nucleophiles whose conjugate acids are strong acids – think pKa < 0 ]. [Note #2]
آیا می توانید با افزودن NaOH به محلول اسید آبی مشکل کوچکی ببینید؟ به نظر شما چه اتفاقی ممکن است بیفتد؟
کبوم. خب این یک اغراق است. اما اسید به طور برگشت ناپذیر NaOH را پروتونه می کند و به ما H می دهد2O [recall that acid-base reactions are fast]. به طور مشابه، می توانید تصور کنید که با افزودن NaNH چه اتفاقی می افتد2 به اسید یا معرف های گریگنارد به اسید: هسته دوست پروتونه می شود و اسید مزدوج را به ما می دهد.
5. در مورد باز کردن تحت شرایط اولیه چطور؟
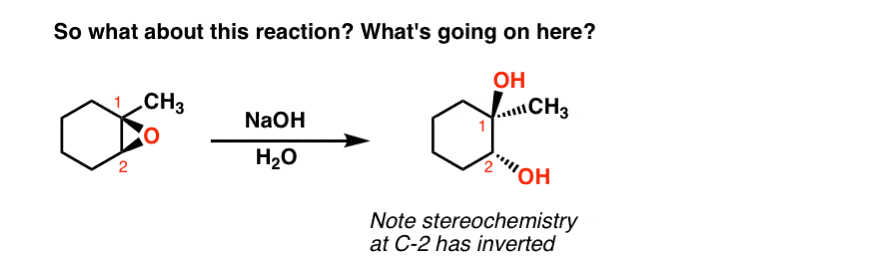
هنوز یک راز برای حل وجود دارد. از آخرین پست ممکن است به خاطر بیاورید که اگر فقط NaOH – بدون اسید – را به اپوکسیدی که در بالا دیدیم اضافه کنیم، کلاً محصول متفاوتی دریافت می کنیم.
توجه داشته باشید که چگونه استریوشیمی در C-2 با اسید کاملاً متفاوت است.
چه اتفاقی ممکن است در اینجا بیفتد؟ هر فکری؟ نکته – این واکنشی است که قبلاً در مورد آن صحبت کرده ایم و حتی در این پست به آن اشاره شده است.
در پست بعدی در این مورد صحبت خواهیم کرد.
پست بعدی – باز کردن اپوکسیدها با پایه
یادداشت
یادداشت 1: چرا هسته دوست به کربن جایگزین بیشتر حمله می کند؟
- در اپوکسید پروتونه شده ما، اگرچه اکسیژن بار رسمی مثبت دارد، اما در حقیقت چگالی بار مثبت بیشتر روی کربن است. [recall that oxygen is more electronegative than carbon].
- به یاد داشته باشید که بار مثبت به بهترین وجه توسط کربن به ترتیب سوم > ثانویه > اولیه تثبیت می شود. بنابراین در مورد ما، اتم کربن سوم بار مثبت بیشتری را تحمل می کند. کربن سوم از نظر الکترون فقیرتر خواهد بود (الکتروفیل)
- طول پیوندهای CO مساوی نخواهد بود – پیوند CO به کربن سوم طولانی تر و ضعیف تر از کربن ثانویه است.
خط پایین: کربن سوم الکتروفیل تر است (الکترون ضعیف) و پیوند CO روی کربن سوم ضعیف تر، طولانی تر و راحت تر شکسته می شود.
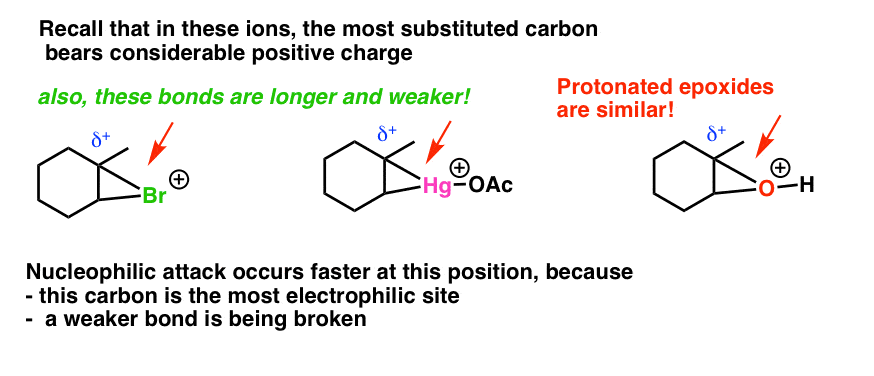
این نمودارها توسط مت مک اینتاش در همین زمینه بسیار مفید هستند. [back to discussion]
(پیشرفته) مراجع و مطالعه بیشتر
- مکانیسم های واکنش های اپوکسید
E. Parker و NS Isaacs
بررسی های شیمیایی 1959، 59 (4)، 737-799
DOI: 10.1021/cr50028a006
این بررسی قدیمی است اما با اصول اولیه در بحث واکنش های اپوکسیدها شروع می شود. هر دو واکنش اسیدی و بازی (نوکلئوفیل) پوشش داده شده است. - روشها و واکنشهای مصنوعی؛ 681. هیدراسیون و متانولیز اپوکسیدها با کاتالیزور Nafion-H
جورج A. Olah، الکساندر P. Fung، دیوید Meidar
سنتز 1981; 1981 (4): 280-282
DOI: 1055/s-1981-29414
در این مثال، NafionTM-H (یک رزین پلیمری که توسط DuPont ساخته شد و متعاقباً توسط پروفسور Olah به فرم سوپراسیدی “-H” تغییر یافت) می تواند به عنوان یک کاتالیزور برای ترویج باز شدن حلقه هیدرولیتیک اپوکسیدها به 1،2-دیول ها استفاده شود. - Friedel-Crafts آلکیلاسیون آرن ها با مونو و بیس(تری فلورومتیل) اکسیران ها در محیط سوپراسید: سنتز آسان آلفا-(Trifluoromethyl)- و α,α-Bis(Trifluoromethyl)-β-Arylethanols
K. Surya Prakash، Pablo J. Linares-Palomino، Kevin Glinton، Sujith Chacko، Golam Rasul، Thomas Mathew و George A. Olah
سینلت 2007، (7) 1158-1162
DOI: 10.1055/s-2007-977423
در شرایط اسیدی برونستد، اپوکسیدها را می توان به عنوان الکتروفیل در واکنش های فریدل کرافت استفاده کرد. - حلقه ترویج شده با آب گرم – باز کردن اپوکسیدها و آزیریدین ها توسط آب و دیگر هسته ها
ژی وانگ، یونگ تائو کوی، ژائو بینگ ژو و جین کو
مجله شیمی آلی 2008، 73 (6)، 2270-2274
DOI: 1021/jo702401t
عنوان دارای این اشتباه تایپی است که من را کمی مشکوک می کند. از سوی دیگر، این یک است JOC مقاله، پس آن را باید قابل اعتماد باشد معلوم می شود که آب گرم می تواند اپوکسیدها را به دیول ها هیدرولیز کند، بدون نیاز به کاتالیزور!اپوکسیدها در هر دو شرایط اسیدی و بازی – یعنی در شرایط واکنش الکتروفیلیک و نوکلئوفیلیک – می توانند تحت باز شدن حلقه قرار گیرند. برای برداشتن این یک قدم جلوتر، در شرایط اسیدی، اپوکسیدها را می توان با هر دو اسید برونستد و لوئیس فعال کرد. کاتالیز اسید لوئیس رایج تر است و در نشریات زیر توضیح داده شده است: - دهانه های هسته دوست با واسطه ایزوپروکسید تیتانیوم از الکل های 2،3-اپوکسی. یک روش ملایم برای باز کردن حلقه انتخابی
موریس کارون و کی بی شارپلس
مجله شیمی آلی 1985، 50 (9)، 1557-1560
DOI: 1021/jo00209a047 - کاتالیز نامتقارن واکنش های باز شدن حلقه اپوکسید
اریک ان. جاکوبسن
حساب های تحقیقات شیمیایی 2000، 33 (6)، 421-431
DOI: 1021/ar960061v
پروفسور ژاکوبسن (هاروارد) با توسعه و مطالعه واکنش های نامتقارن شغلی ایجاد کرده است. یکی از کمک های قابل توجه او توسعه یک کاتالیزور کروم (سالن) برای باز شدن حلقه نامتقارن اپوکسیدها است و داستان توسعه این شیمی در اینجا شرح داده شده است. - باز شدن اپوکسید با ترت بوتیل دی متیل سیلیل سیانید- روی یدید. شواهدی برای یک فرآیند گام به گام در باز کردن یک اپوکسید با مانع فضایی
پل جی گسمن و لئونارد ام هابرمن
مجله شیمی آلی 1986، 51 (25)، 5010-5013
DOI: 1021/jo00375a050
این مطالعه یک واکنش غیرمعمول اما جالب است که در آزمایشگاههای پروفسور PG Gassman فقید (U Minnesota) ایجاد شده است. واکنش اپوکسیدها با TMSCN (جایگزینی محلول در آلی و کارکرد آسان تر برای معرف های سنتی سیانید مانند KCN) و ZnI کاتالیزوری2 1،2 می دهد –ایزوسیانو الکل ها این مقاله بررسی مکانیکی این واکنش است. - تبدیل اپوکسیدها به β-هیدروکسی ایزوسیانیدها: trans-2-ISOCYANOCYCLOHEXANOL
پل جی گسمن و توماس ال. گوگنهایم
سازمان مصنوعی. 1986، 64، 39
DOI: 10.15227/orgsyn.064.0039
یک سنتزهای آلی روش برای باز کردن حلقه اپوکسیدها به الکل های 1،2-ایزوسیانو.
