در اینجا نکته ای وجود دارد که باعث سردرگمی زیادی می شود.
به این دو واکنش نگاه کنید. به نظر شما پیوند قوی تر، OH یا CH چیست؟
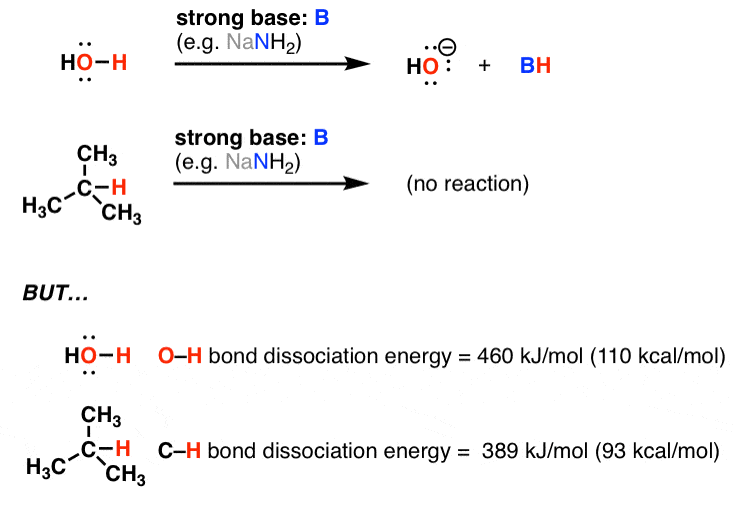
بر اساس این جدول (PDF) انرژی تفکیک پیوند (BDE) OH 460 کیلوژول بر مول (110 کیلوکالری در مول) و مقدار CH 389 کیلوژول بر مول (93 کیلو کالری بر مول) است. [For another table, see this page from Reusch]. پس چرا پیوند قویتر در اینجا شکسته میشود؟
مثالی دیگر:
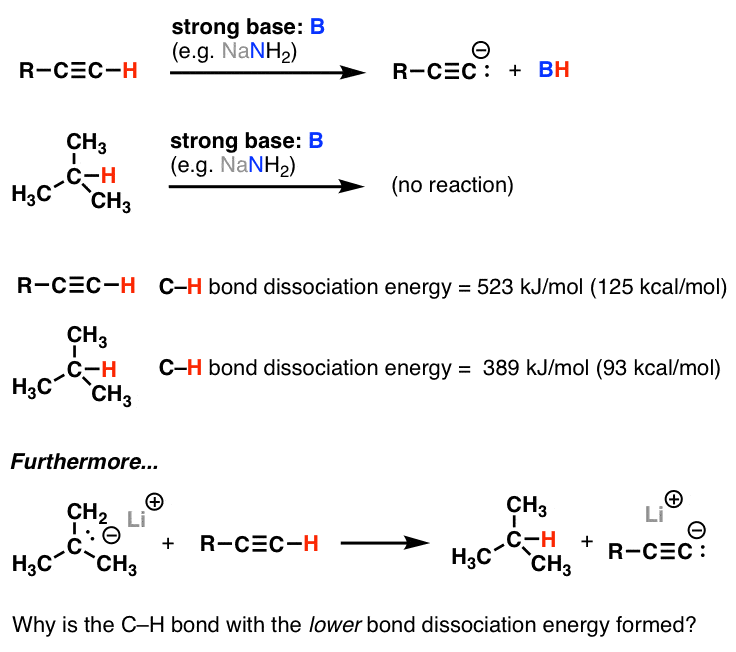
اما استحکام باند در اینجا آلکین CH (523 kJ/mol یا 125 kcal/mol) در مقابل استحکام باند سوم CH در این مورد (384 kJ/mol یا 93 kcal/mol) است. بنابراین چرا پیوند CH با انرژی تفکیک پیوند پایین تر تشکیل می شود و پیوند CH بالاتر شکسته می شود؟
در اینجا سه سرنخ در مورد انرژی های تفکیک پیوند آورده شده است.
1) برای پیوندهای CH، با اضافه کردن جایگزینی به کربن، انرژی تفکیک پیوند کاهش می یابد.
2) آب می تواند در واکنش های اسید-باز دخالت کند، اما water تمایل به تداخل با واکنش های رادیکال آزاد ندارد. اگر واکنش گریگنارد را در آزمایشگاه انجام داده باشید، میدانید که آنها چقدر میتوانند سخت باشند، زیرا برای شروع باید تمام آثار آب را از حلال حذف کنید. از طرف دیگر، همین محدودیت برای واکنش های رادیکال آزاد اعمال نمی شود! میتوان واکنشهای رادیکال آزاد را در حضور آب بدون نگرانی از اینکه واکنش رادیکال آزاد مورد نظر توسط H-OH به دام افتاد، انجام داد.
3) سرنخ دیگر این است که تشکیل رادیکال های آلکیل بسیار آسان تر از آلکنیل و آلکینیل است.
پاسخ این است که انرژی تفکیک پیوند = شکاف همولیتیک
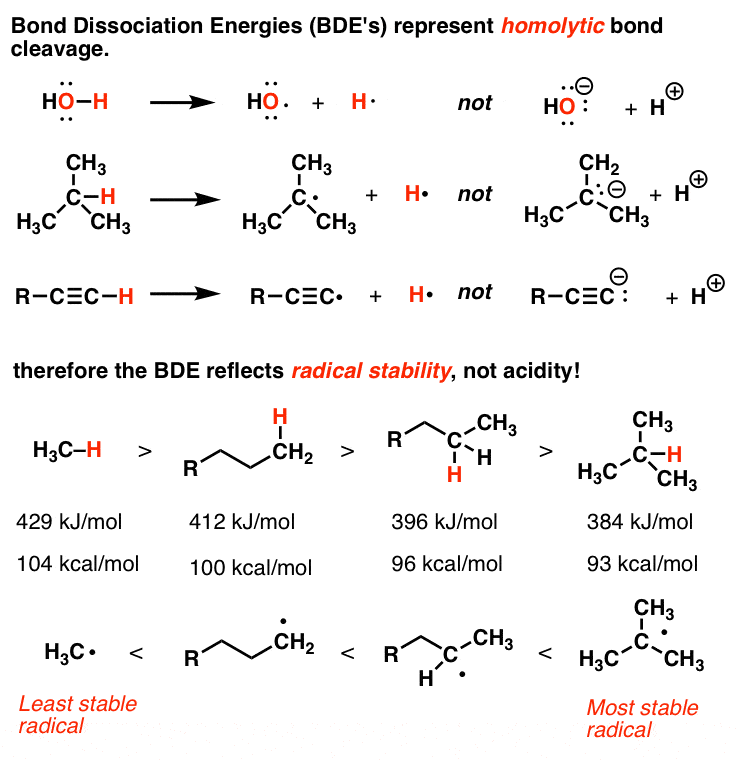
انرژی های تفکیک پیوند اندازه گیری شده (BDE) در جداول نشان دهنده تجزیه پیوند به دو بخش است. رادیکال ها. این به دلیل روشی است که انرژی های تفکیک پیوند اندازه گیری می شود – از طریق کالری سنجی واکنش های رادیکال.
بنابراین انرژی تفکیک پیوند نشان دهنده ثبات رادیکال های تشکیل شده است! R3C• یک رادیکال پایدارتر از HO• است. R3C• همچنین یک رادیکال پایدارتر از یک رادیکال آلکینیل است. همچنین به توضیح اینکه چرا ترتیب استحکام باند به CH اولیه > CH ثانویه > CH ثالثیه میرود کمک میکند.
PS چرا هستند همولیتیک استحکام باند اندازه گیری شد و نه هترولیتیک? این سوال خوبی است. شکستن پیوندهای CH و CC در آلکان ها به صورت همولیتیک بسیار ساده تر است. ثانیاً، رادیکالها خنثی هستند و مانند آنیونها، یک پوسته حلال را با خود حمل نمیکنند. بنابراین نسبت به اثرات حلال حساسیت کمتری دارند. برای بحث فنی، اینجا را ببینید.
PPS چرا رادیکال OH ممکن است از رادیکال های R پایدارتر باشد و پایداری رادیکال های آلکیل بیشتر از رادیکال های آلکنیل و آلکینیل باشد؟
(پیشرفته) مراجع و مطالعه بیشتر
- کاستیهای مبتنی بر انرژیهای تثبیت رادیکالی بر انرژیهای تفکیک پیوند گروههای آلکیل به هیدروژن
آندریاس آ. زاویتسا، دونالد دبلیو راجرز و نیکیتا ماتسوناگا
مجله شیمی آلی 2010، 75 (16)، 5697-5700
DOI: 1021/jo101127m
چندین کتاب درسی، از جمله برخی از کتابهای پیشرفته، انرژیهای تثبیتکننده رادیکال را ارائه میکنند، و این مقاله به این موضوع میپردازد که چرا این ممکن است بهترین راه برای تعیین کمیت پایداری رادیکالهای آزاد نباشد. - در مورد مزایای انرژی های تثبیت رادیکال هیدروکربنی بر اساس انرژی های تفکیک پیوند R-H
متیو دی. وودریچ، دبلیو. چاد مک کی، و پل فون راگو شلایر
مجله شیمی آلی 2011، 76 (8)، 2439-2447
DOI: 1021/jo101661c
این مقاله به برخی از کاستیهای رویکرد استفاده شده در شماره 1 در بالا میپردازد. مرحوم پروفسور شلایر شخصیت بسیار تأثیرگذاری در شیمی آلی بود و در استفاده از روش های محاسباتی برای حل مسائل جالب در شیمی آلی پیشگام بود. - انرژی تثبیت رادیکال یک رادیکال آزاد کربن محور جایگزین هم به عملکرد جانشین و هم به عادی بودن رادیکال بستگی دارد.
ماروین ال. پوتسما
مجله شیمی آلی 2011، 76 (1)، 270-276
DOI: 1021/jo102097n - یک مقیاس جهانی واحد از انرژیهای تثبیت رادیکال وجود ندارد: انرژیهای تفکیک پیوند جهانی و ترموشیمی رادیکال با ترکیب دو مقیاس جهانی توصیف میشوند.
آندریاس آ. زاویتزاس
مجله شیمی آلی 2008، 73 (22)، 9022-9026
DOI: 1021/jo8018768 - انرژی های تفکیک پیوند با روش های جنبشی
A. Kerr
بررسی های شیمیایی 1966، 66 (5)، 465-500
DOI: 10.1021/cr60243a001
این مقاله تکنیکهای تجربی برای اندازهگیری BDEs همولیتیک را شرح میدهد. - III – انرژی های پیوند
سیدنی دبلیو بنسون
مجله آموزش شیمی 1965، 42 (9)، 502
DOI: 10.1021/ed042p502
این مقاله اندازهگیری تجربی انرژیهای تفکیک پیوند همولیتیک را توصیف میکند. این مقاله توسط پروفسور بنسون در زمانی که در موسسه تحقیقاتی استنفورد (در حال حاضر SRI International)، یک مرکز تحقیقاتی غیرانتفاعی بسیار نزدیک به دانشگاه استنفورد، نوشته شده است. در سال 1978، پروفسور بنسون به پروفسور جورج اولاه در USC پیوست و به تأسیس موسسه تحقیقاتی هیدروکربن لوکر در آنجا کمک کرد. - از اسیدیته های تعادلی گرفته تا انرژی های تثبیت کننده رادیکال
فردریک جی. بوردول و شیان من ژانگ
حساب های تحقیقات شیمیایی 1993، 26 (9)، 510-517
DOI: 10.1021/ar00033a009
این مقاله سعی می کند اسیدیته یک پروتون را با BDE پیوند CH یا XH مربوطه مرتبط کند. - محاسبات Ab Initio انرژیهای تثبیت تشدید نسبی رادیکالهای آلیل و بنزیل
دیوید ا.هروات و وستون تاچر بوردن
مجله شیمی فیزیک 1994، 98 (41)، 10460-10464
DOI: 1021/j100092a014
انرژی تثبیت یک گروه وینیل (در رادیکال آلیل) و یک گروه فنیل (در رادیکال بنزیل) به ترتیب 7/15 کیلوکالری بر مول و 5/12 کیلوکالری بر مول محاسبه شده است. - تأثیر پذیرندگان و اهداکنندگان مجاور بر پایداری رادیکالهای کربن محور
G. Bordwell، Xianman Zhang، و Mikhail S. Alnajjar
مجله انجمن شیمی آمریکا 1992، 114 (20)، 7623-7629
DOI: 10.1021/ja00046a003
جدول I در این مقاله حاوی انرژی های تثبیت رادیکال های متیل با جایگزین های مختلف است (به عنوان مثال ·CH2ایکس).
