الکترون های ظرفیت کربن در مورد پیوند در CH به ما چه می گویند4?
(نکته: از لحظه دوقطبی CH4 صفر است، پاسخ این است، “کافی نیست”)
اگر پیکربندی مداری کربن 2 ثانیه باشد22p2 ، پس چگونه می توانیم از این اطلاعات برای فهمیدن اینکه آرایش اوربیتال ها در یک مولکول آلی ساده مانند متان (CH) استفاده کنیم.4)؟
معلوم شد که متان چهار وجهی است، با 4 زاویه پیوند مساوی 109.5 درجه و 4 طول پیوند مساوی و بدون گشتاور دوقطبی.
این دو سوال را پیش می آورد. اول، چگونه ما دانستن که CH4 چهار وجهی است؟ و ثانیا، چگونه این پیکربندی الکترونیکی را با هم تطبیق دهیم (2s22p2 ) با این واقعیت که داریم چهار پیوندهای مساوی C-H؟
1. پیکربندی الکترونیکی الکترون های ظرفیت کربن 2s است22p2
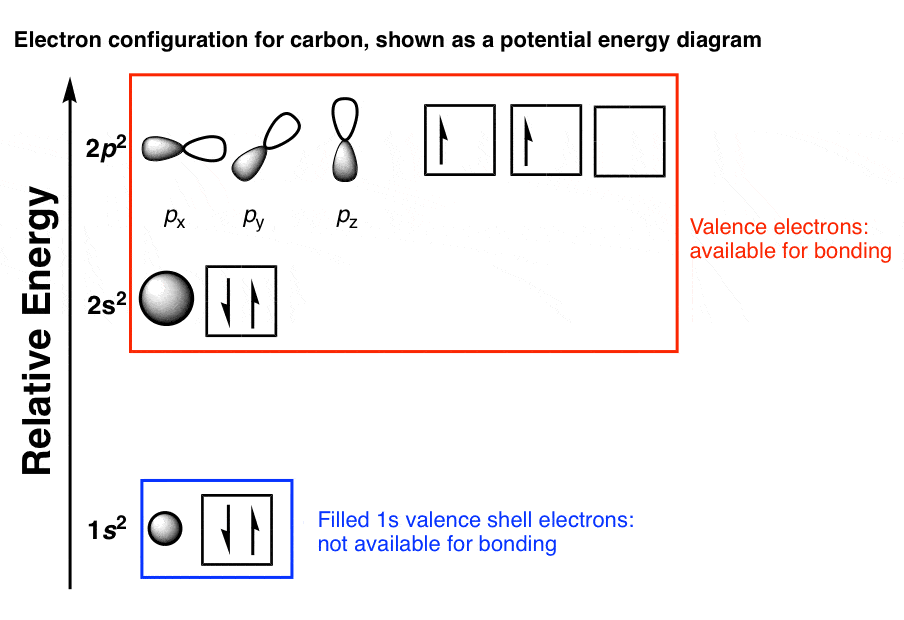
در بررسی اوربیتال های اتمی، دیدیم که پیکربندی مداری اتمی الکترون های ظرفیت کربن 2 ثانیه است22p2 همانطور که در زیر نشان داده شده است:
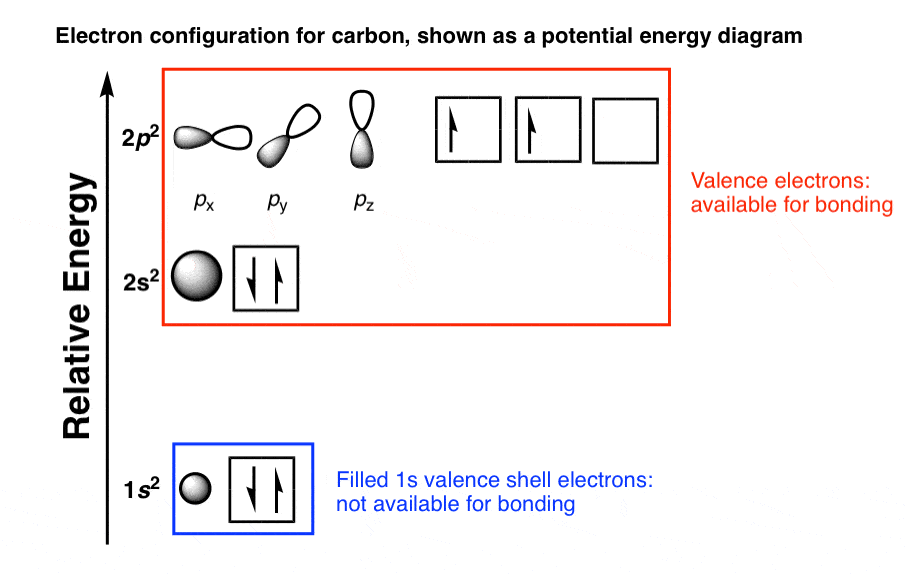
از آنجایی که اوربیتال 2s انرژی کمتری نسبت به 2p دارد، ابتدا پر می شود. یعنی دو الکترون در اوربیتال 2s و یک الکترون در دو تا از سه اوربیتال 2p وجود دارد. یک اوربیتال 2p خالی نیز وجود دارد.
[In addition, there are two electrons in the “inner shell” 1s orbital, which are not available for bonding].
2. آیا می توانیم از این اطلاعات برای کشف ساختار متان استفاده کنیم (CH4)؟ (اسپویل: نه)
تا اینجای کار خیلی خوبه. اگر فقط در مورد اتم های کربن جدا شده صحبت کنیم، خوب است.
اما برای اینکه واقعا مفید باشیم، باید بتوانیم مدارهای کربن را با ساختار و پیوند ترکیبات آلی واقعی مرتبط کنیم.
ساده ترین ترکیب آلی متان، CH است4. پس بیایید چهار اتم هیدروژن را در تصویر بیاوریم و سعی کنیم آنچه را که آموختهایم به کار ببریم تا به فرضیههایی درباره پیوند در این مولکول برسیم.
3 اوربیتال p در کربن همگی در 90 درجه نسبت به یکدیگر، در امتداد محورهای x، y و z قرار دارند.
آیا نباید انتظار داشته باشیم که ساختار متان دارای سه پیوند CH برای هر یک از اوربیتال های p (در 90 درجه نسبت به یکدیگر) و سپس چهارمین پیوند CH متصل به اوربیتال 2s باشد؟ از آنجایی که جفت های الکترون دفع می کنند، شاید باید آن پیوند CH را حداکثر فاصله از سایر پیوندهای CH قرار دهیم. این یک زاویه پیوند H-C-H 135 درجه ایجاد می کند.
با پیروی از این منطق، ساختاری مانند این ایجاد می شود:
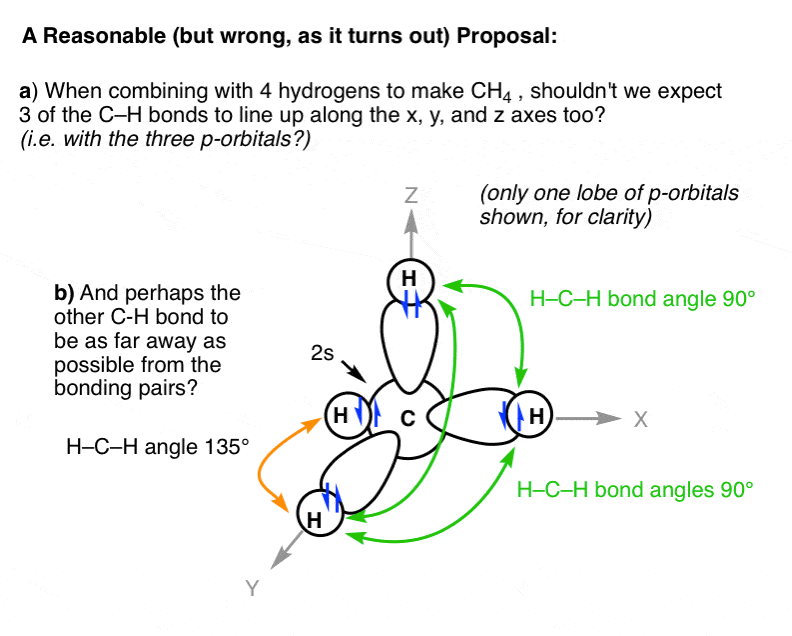
همانطور که پیداست، می توان نشان داد که این پیشنهاد اشتباه است.
چرا؟
لحظه دوقطبی
به یاد بیاورید که هر پیوند C-H به دلیل تفاوت در الکترونگاتیوی بین C (2.5) و H (2.2) دوقطبی کوچک دارد. انتظار داریم C تا حدی منفی و H تا حدی مثبت باشد.
- اگر ساختار فوق دقیقاً ساختار متان را به تصویر میکشید، انتظار میرفت که متان 3 پیوند C-H طولانیتر (به اوربیتالهای 2p) و یک پیوند C-H کوتاهتر (به اوربیتال 2s که به هسته نزدیکتر است) داشته باشد.
- علاوه بر این، ما انتظار داریم 3 زاویه پیوند H–C–H 90 درجه و یک زاویه پیوند H–C–H 135 درجه باشد.
- هنگامی که مجموع بردار دوقطبی های C-H در این ساختار جمع می شوند، این کار را انجام می دهند نه همه لغو
- بنابراین انتظار داریم یک گشتاور دوقطبی کوچک اما قابل اندازه گیری برای CH مشاهده کنیم4. [Note 1]
با این حال گشتاور دوقطبی اندازه گیری شده CH4 صفر است. بنابراین این ساختار نمی تواند درست باشد.
این به ما می گوید که تمام طول های پیوند و زوایای پیوند در متان یکسان هستند.
3. شاید متان (CH4) آیا مربع مسطح است؟
باشه میگی اگر تمام پیوندهای CH دارای طول و زاویه مساوی هستند، چرا نمی توان CH را انجام داد4 ساختار زیر را داشته باشید، جایی که تمام زوایای پیوند 90 درجه و CH هستند4 صاف، در صفحه صفحه است. (ما این ساختار را “مسطح مربع” می نامیم).

این در واقع تا حدود سال 1880 نظر اکثریت برای چیدمان پیوندها در اطراف کربن بود. شیمیدانان بسیار درخشانی مانند برزلیوس به گور آنها رفتند و دلیلی برای شک نداشتند که متان چیزی جز صاف است.
با این حال، اکنون می دانیم که این اشتباه است. چرا؟
4. رد ساختار مربع مسطح CH4 (1874) و پیشنهاد یک ساختار چهار وجهی
اگر متان به گونهای اصلاح شود که کربن مرکزی به چهار گروه مختلف متصل شود، مولکول میتواند بهعنوان دو ایزومر مختلف وجود داشته باشد که تصاویر آینهای غیرقابل نصب هستند (این “ایزومر نوری” نامیده میشود و بعداً پوشش داده میشود).
این در صورتی امکان پذیر است که آرایش 4 گروه در اطراف کربن مرکزی چهار وجهی باشد، اما نه اگر مولکول مربع مسطح باشد. به عنوان مثال، برموکلروفلوئورومتان مشتق متان دارای چهار گروه مختلف در اطراف کربن است و می تواند به دو ایزومر مختلف جدا شود که نور پلاریزه شده صفحه را در جهات مختلف می چرخانند. [As we’ll see later, these isomers are called “enantiomers”]
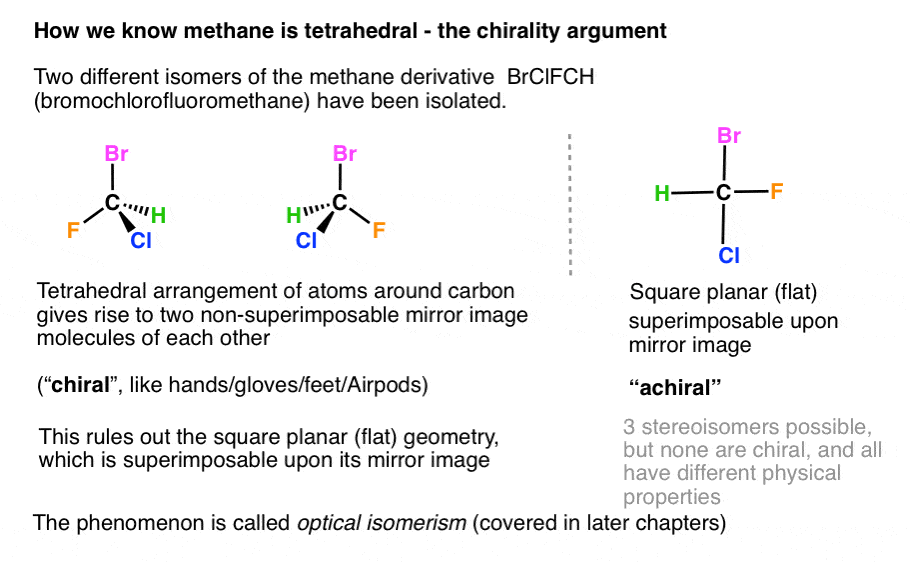
این مشاهدات ساختار مسطح مربع را رد می کند. اگر کربن مسطح مربع بود، مولکول مسطح بود و روی تصویر آینهای خودش قرار میگرفت و فقط یک ایزومر امکانپذیر بود.
Jacobus Henricus van’t Hoff، یکی از همکاران کالج دامپزشکی در اوترخت، از اولین کسانی بود که به احتمال کربن سه بعدی پرداخت. او در «La Chimie dans L’Espace» (1874) اشاره کرد که آرایش اتمها در فضا پیامدهای عملی مهمی دارد – نکتهای که تا آن زمان کاملاً نادیده گرفته شده بود. وانت هاف نشان داد که آرایش چهار ضلعی از چهار گروه مختلف در اطراف یک اتم کربن (که او آن را “کربن نامتقارن” نامید) دو ایزومر متفاوت ایجاد می کند، و علاوه بر این، این توضیح می دهد که چرا اسید تارتاریک (با دو اتم کربن نامتقارن). ) به سه شکل (+، – و.) وجود داشت مزو). [Source]

کار وانت هاف – که باید توجه داشت صرفاً نظری بود – در برخی محافل مورد استقبال قرار نگرفت.
5. کربن های چهار وجهی: ایده ای رایج در سال 1874 نیست
شیمیدان برجسته آلمانی هرمان کولبه چنین گفته است:

به نوبه خود، وانت هاف با پگاسوس خود به استکهلم پرواز کرد تا اولین جایزه نوبل شیمی را در سال 1901 دریافت کند. [Note 2]
در سال 1913، زمانی که براگ ساختار الماس را با استفاده از کریستالوگرافی اشعه ایکس تعیین کرد و دریافت که آن یک شبکه چهار وجهی از اتم های کربن با زاویه پیوند CCC 109.5 درجه است، اثبات غیرقابل انکار برای آرایش چهار وجهی پیوندهای اطراف اتم کربن ارائه شد.
6. بنابراین چه اوربیتال ها درگیر هستند؟
ما اکنون آرایش چهار وجهی اتم ها در اطراف متان را به دلیل دافعه جفت های پیوندی الکترون ها با یکدیگر (معروف به نظریه VSEPR) منطقی می کنیم.
این به ما در درک این کمک نمی کند اوربیتال ها با این حال درگیر در پیوند است.
اگر بپذیریم که آرایش هیدروژنها در اطراف متان چهار وجهی است، با توجه به اطلاعاتی که در مورد هندسه متان داریم، چگونه اوربیتالهای پیوند متان را توصیف کنیم. س و پ اوربیتال ها؟
از این گذشته، اوربیتال های 2p همگی در 90 درجه نسبت به یکدیگر قرار دارند، اما زوایای پیوند در متان 109.5 درجه است.
علاوه بر این، چگونه محاسبه کنیم که هر یک از 4 پیوند موجود در متان دارای طول یکسانی هستند؟ مثلاً اوربیتال 2s چه شد؟
آیا الکترون های موجود در پیوندهای CH در نظر گرفته می شوند؟ پ اوربیتال ها یا س اوربیتال ها؟ یا چیز دیگری؟
همانطور که به نظر می رسد، درمان مرسوم این است که با پیوندهای اطراف کربن به صورت درون برخورد شود اوربیتال های ترکیبی
اطلاعات بیشتر در مورد آن در پست بعدی
پست بعدی: اوربیتال های ترکیبی
یادداشت
یادداشت 1. توجه داشته باشید که متان تک دوتره (CH3D، جایی که D دوتریوم است، ایزوتوپ سنگین هیدروژن) دارای یک گشتاور دوقطبی کوچک است که اندازه گیری شده است. [ref]
تبصره 2: لازم به ذکر است که جایزه نوبل وانت هاف به دلیل کمک های او در شیمی فیزیک است نه استریوشیمی آلی.
من مدیون این صفحهای هستم که کتاب «آرایش اتمها در فضا» وانت هاف را برای دیدگاه تاریخی پوشش میدهد. ارزش خواندن کامل را دارد
از همین منبع: مدل های چهار وجهی van’t Hoff [from the Leiden history of science museum; source]

از همان نویسنده، دیدگاه تاریخی بیشتری در مورد شکاف کلبه/وانت هوف:
بدیهی است که کولب احمقانه بود که تا این حد بیاعتنا و کینه توز بود. او هم کوته فکر بود و اشتباه حدس می زد. ما به راحتی می توانیم درک کنیم که او در دادگاه تاریخ آنچه را که به سراغش می آمد به دست آورد.
چالش به درستی احترام گذاشتن به مشارکت های ضروری نگرش او برای توسعه شیمی است. با نزدیک شدن به مشاهدات تجربی دقیق بود که شیمی به جایی که بود (و هست) رسیده بود. کولبه تلاش می کرد علم را در مسیری سازنده و قابل توجیه عقلانی نگه دارد.
برای کامل اینجا را بخوانید.
