واکنشهای حذف (E1) که با بازآراییها رخ میدهد – تغییرات هیدرید یا آلکیل
در جایی که کربوکاتیونها وجود دارند (به پست آخر مراجعه کنید)، واکنشهای بازآرایی هرگز عقبتر نیستند. دوستان قدیمی ما برای یک بازدید کوتاه در این فصل در مورد واکنش های حذف بازگشته اند.
فهرست مطالب
- چه چیزی در مورد این واکنش حذفی عجیب است؟
- حذف (E1) با Hydride Shift
- حذف (E1) با تغییر آلکیل
- (پیشرفته) مراجع و مطالعه بیشتر
1. چه چیز عجیبی در مورد این واکنش حذف وجود دارد؟
آخرین واکنش (عجیب) برای نشان دادن شما در مورد واکنش های حذف. می توانید ببینید چه چیز عجیبی در آن وجود دارد؟
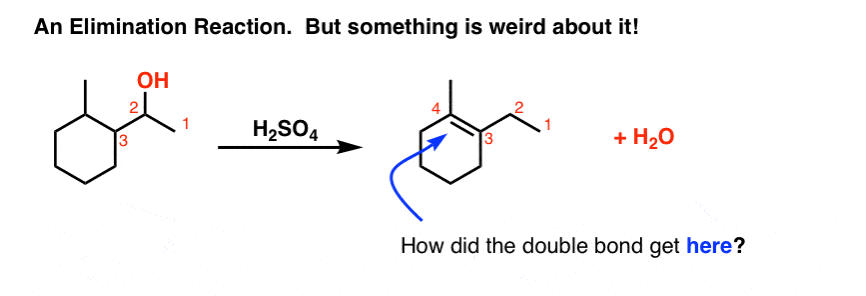
چگونه آن پیوند دوگانه از بین رفت آنجا؟ معمولاً وقتی حذف اتفاق می افتد، هیدروژنی را از کربن مجاور گروه خروجی حذف می کنیم. اما در اینجا، یک چیز اضافی رخ داده است.
2. حذف (E1) با بازآرایی: Hydride Shift
بیایید به همه پیوندهایی که شکل می گیرند و پیوندهایی که شکسته می شوند نگاه کنیم تا بتوانیم ردیابی کنیم دقیقا چه اتفاقی می افتد:
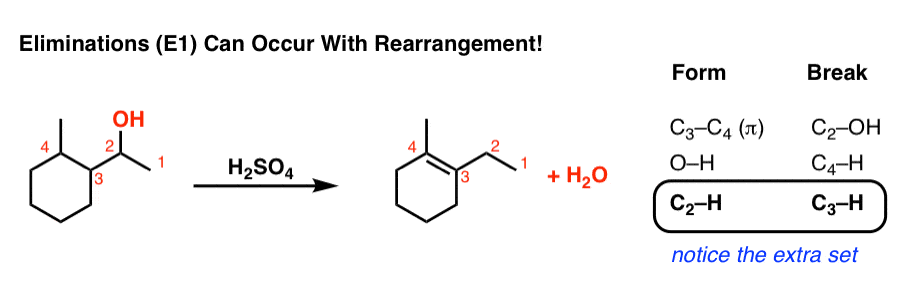
توجه کنید که چگونه با یک واکنش حذف معمولی متفاوت است؟ مطمئناً، ما در حال تشکیل CC (π) و شکستن CH و C-OH هستیم، اما یک CH اضافی داریم که تشکیل میشود و یک CH اضافی که میشکند.
این یک نشانه مطمئن از یک مرحله بازآرایی است!
پس اینجا چه خبر است؟
خوب، ما با پروتونه کردن الکل شروع می کنیم. این اجازه می دهد تا آب در مرحله بعدی که یک کربوکاتیون را تشکیل می دهد، خارج شود. موضوع اینجاست: کربوکاتیون است ثانوی، و ما در مجاورت a هستیم درجه سوم کربن. بنابراین اگر هیدروژن (و جفت الکترون های آن) از C3 در مثال ما به C-2 مهاجرت کنند، اکنون یک کربوکاتیون سوم خواهیم داشت که پایدارتر. سپس، یک پایه (آب در این مثال) می تواند CH را حذف کند و آلکن جایگزین بیشتری را تشکیل دهد (محصول Zaitsev در این مورد). و اینگونه است که آلکن به آنجا ختم می شود.
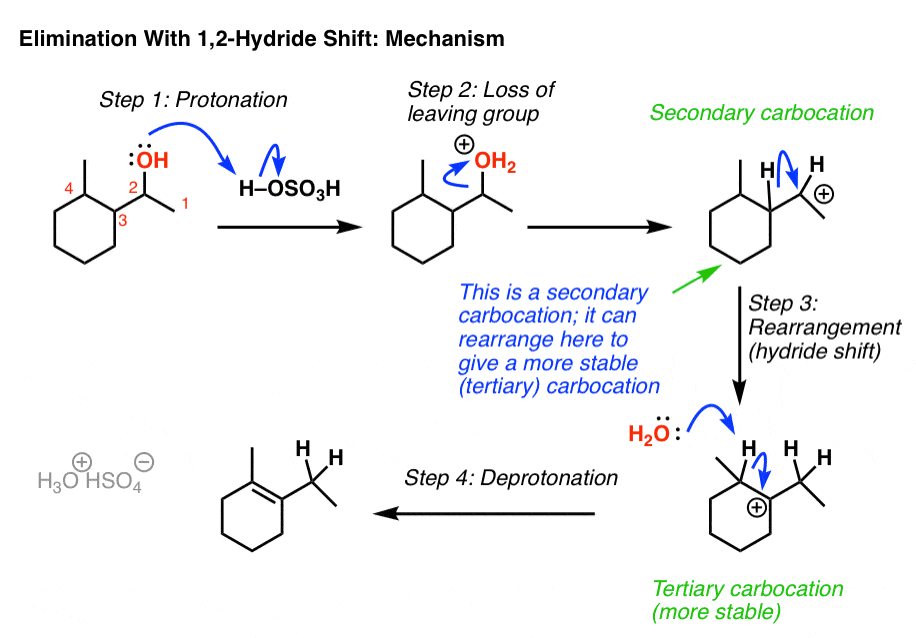
خوب. بنابراین این یک معما حل شده است.
3. حذف (E1) با بازآرایی: Alkyl Shift
شاید به خاطر داشته باشید که این نوع بازآرایی ها می توانند در واکنش های SN1 نیز رخ دهند. و اگر آن پست را بخوانید، ممکن است به یاد بیاورید که علاوه بر جابجایی هیدروژن («هیدرید»، زیرا یک جفت الکترون به آن متصل است) میتوانیم جابجایی آلکیل نیز داشته باشیم. در اینجا یک مثال نهایی است. توجه – من هم یک ویدیو از این ساخته ام، می توانید آن را اینجا ببینید.
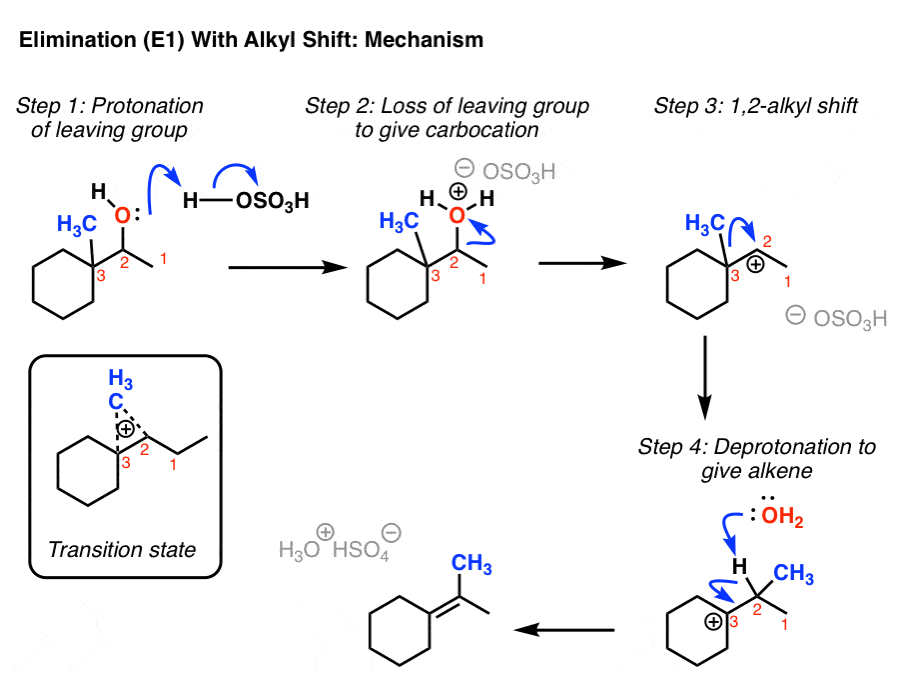
این تقریباً این کار را برای واکنش های حذف انجام می دهد.
در سری بعدی پستها، بیایید یکی از بزرگترین سوالاتی که دانشآموزان با آن دست و پنجه نرم میکنند را بررسی کنیم. خوب، اکنون که واکنشهای جایگزینی و حذفی را پشت سر گذاشتهایم، چگونه تصمیم میگیریم که کدام یک در هر موقعیتی رخ دهد؟
سوال عالی بعدش همینه
(پیشرفته) مراجع و مطالعه بیشتر
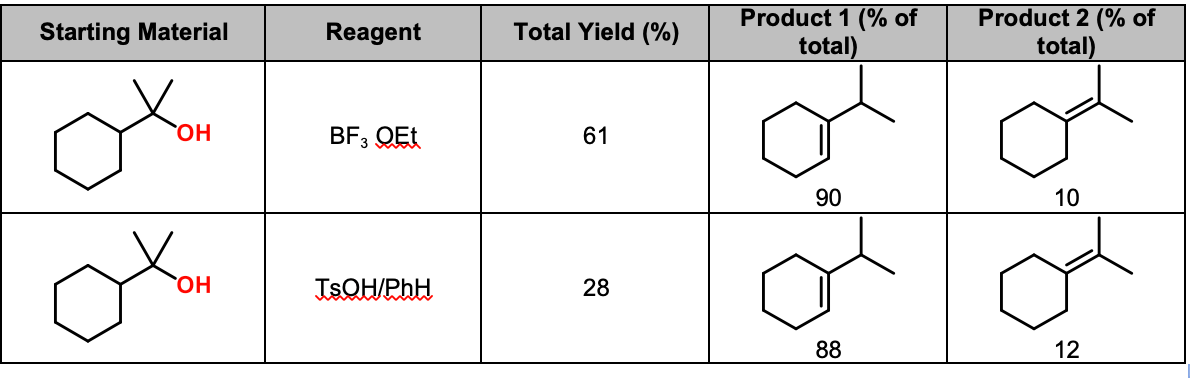
- این مقاله را برای نمونه های بسیار تمیز و کلاسیک کم آبی با تغییر آلکیل بررسی کنید. نویسندگان 1-سیکلوهگزیل-1-متیل اتانول را می گیرند و آن را با TsOH/بنزن یا BF3•OEt درمان می کنند.2. ممکن است فکر کنید که آنها الفین چهار جایگزین را دریافت می کنند، اما محصول غالب آلکن سه جایگزین است (90:10). دلیل اسیدیته بیشتر پیوندهای CH محوری است که با کربوکاتیون میانی همسو هستند.
BF3·OEt2 باعث کاهش سریع، خفیف، تمیز و انتخابی منطقه ای الکل های سوم می شود.
پوزنر، جی اچ. شولمن-روسکس، EM; اوه، CH; کری، J.-C.; سبز، JV; کلارک، AB; دای، اچ. انژه، ده
چهار وجهی لت. 1991، 32 (45)، 6489-6492.
DOI: 10.1016/0040-4039(91)80200-P
- همسایگی هیدروژن، اثر ایزوتوپی، و ترکیب در حلولیز 3-متیل-2-بوتیل p-تولوئن سولفونات
اس. وینستین، جی. تاکاهاشی
چهار وجهی 1958، 2 (3-4)، 316-321
DOI: 10.1016/0040-4020(58)88053-9
3-متیل-2-بوتیل-توزیلات نمونه ای از سیستمی است که به راحتی تحت حلولیز مجدداً تنظیم می شود که در جدول 3 نشان داده شده است. - مکانیسم های واکنش های حذف سیزدهم. تأثیر باز، حلال و ساختار بر نسبت محصول در واکنش های حذف برخی توزیلات های ثانویه
Irving N. Feit و William H. Saunders
مجله انجمن شیمی آمریکا 1970، 92 (6)، 1630-1634
DOI: 1021/ja00709a035
در پایان، در این مقاله آمده است:نکته جالب توجه در واکنشهای E1 این است که الفینهای حاصل از هیدرید با توسیلاتهای 2-متیل-3-پنتیل و 3-متیل-2-بوتیل، 2-متیل-1-پنتن و 2-متیل-ال-بوتن تغییر میکنند. به ترتیب، در مقادیر فزاینده در امتداد سری حلال n-BuOH “ - مطالعات بازآرایی با C14: نهم فرمولیز متیل-C14-ایزوپروپیل کاربینیل p-تولوئن سولفونات
جی. فینلیسون و سی سی لی
می توان. جی. شیمی. 1960، 38، 787-792
DOI: 10.1139/v60-114
مطالعه دیگری در مورد همین سیستم از Ref. 1، این از C استفاده می کند14 برچسب زدن برای مطالعه روند بازآرایی ها – به صفحه مراجعه کنید. 700. - Über die Pinakolinumlagerung cyclischer Verbindungen
هانس میروین، والتر اونکل
لیب ان شیمی. 1910، 376 (2)، 152-163
DOI: 10.1002/jlac.19103760203
این مقاله توسط Hans Meerwein، پیشگام اولیه در مطالعه کربوکاتیونها و بازآراییهای کاتالیز شده با اسید، در مورد بازآراییهای پیناکول و نیمهپیناکولیک است. در این مقاله، او نشان می دهد که 2،2-دی متیل سیکلوهگزانول توسط اسید به مخلوطی از ایزوپروپیلیدن سیکلوپنتان و 1،2-دی متیل سیکلوهگزن تبدیل می شود. - Über Ringveränderungen bei der Wasserabspaltung aus alicyclischen Alkoholen
هانس میرواین
لیب ان شیمی. 1918، 417 (2-3)، 255-257
DOI: 10.1002/jlac.19184170205 - مبنای مشترک بازآرایی های درون مولکولی. II.1 آبگیری دی ترت بوتیل کربینول و تبدیل نونهای حاصل به تری متی اتیلن و ایزوبوتیلن
فرانک سی ویتمور و ای ای استالی
مجله انجمن شیمی آمریکا 1933، 55 (10)، 4153-4157
DOI: 1021/ja01337a042
پروفسور FC Whitmore در بررسی های مربوط به تاریخچه شیمی کربوکاتیون ذکر شده است، زیرا او اولین کسی بود که پیشنهاد کرد کربوکاتیون ها با یک “جنس باز” از الکترون ها نمایش داده شوند و آنها را به این صورت ترسیم کنند. - مکانیسم جایگزینی در یک اتم کربن اشباع. قسمت بیست و نهم. نقش مانع فضایی (بخش D) مکانیسم واکنش نئوپنتیل بروماید با اتیل الکل آبی
I. داستروفسکی و ED هیوز
جی. شیمی. اجتماعی، 1946، 166-169
DOI: 10.1039/JR9460000166
تحت شرایط استفاده شده در اینجا (اتانول آبی با NaOH)، حدود 36 درصد از الفین بازآرایی شده (تری متیل اتیلن) از نئوپنتیل بروماید به دست آمد. در صورت استفاده از شرایط اسیدی که به نفع تشکیل کربوکاتیون ها است، بازده احتمالی بالاتر الفین امکان پذیر خواهد بود. - تبدیل لانوستان به کوکوربیتان
ادواردز، OE; کلت، آر جی.
می توان. جی. شیمی. 1987، 65 (3)، 595-612.
DOI: 10.1139/v87-104
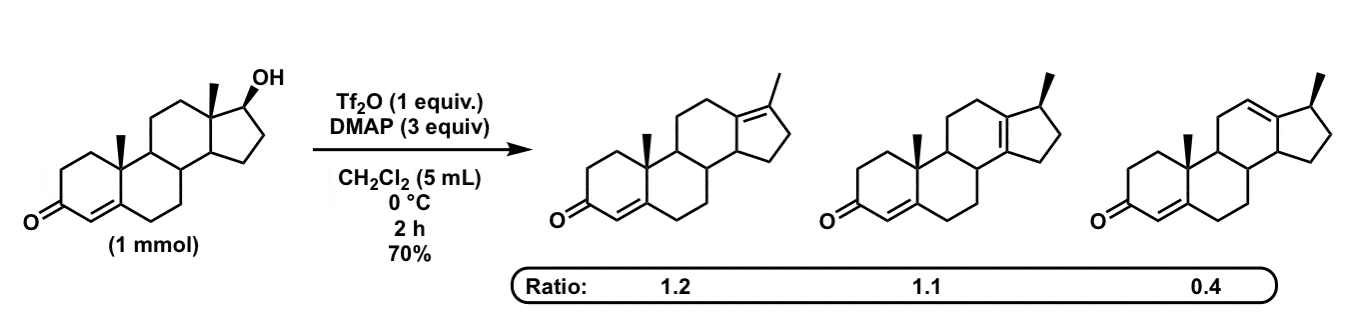
نویسندگان یک سیستم بسیار سفت و سخت (لانوستان استروئیدی) حاوی الکل ثالثیه را انتخاب کردند و مشاهده کردند که وقتی با اسید قوی کم آب شود (H) چه اتفاقی می افتد.2بنابراین4 – AcOH – Ac2ای به اصطلاح “شرایط وستفالن”). پس از از دست دادن آب، یک جابجایی متیل از کربن چهارتایی مجاور مشاهده میشود (جالب یک تغییر هیدرید نیست، جالب است!) و نویسندگان نسبت آلکنها را مقایسه میکنند (سهجانشین شده در مقابل چهار جایگزین). نسبت ها تا حد زیادی تحت تأثیر اثرات الکترونیکی ظریف گروه های راه دور قرار می گیرند. - یک روش خفیف یک گلدانی برای تبدیل الکل های ثانویه استروئیدی مختلف به الفین های مربوطه.
کومار، RR; هاولی، SD; کاگان، اچ بی
سینلت 2011، 2011 (12)، 1709-1712.
DOI: 10.1055/s-0030-1260803
سیستم استروئیدی کمی متفاوت است که مخلوطی از بازآرایی + محصولات حذف را ارائه می دهد.