چهار پست در مورد اسید-باز، جایگزینی، افزودن و حذف، 4 واکنش اصلی در شیمی آلی را پوشش میدهند. در این سری دوم پستها، ما فراتر از اینها میرویم تا تعدادی از واکنشهای کمتر رایج (اما همچنان مهم) را که یاد میگیرید معرفی کنیم. در شیمی آلی 1. دفعه قبل در مورد بازآرایی ها صحبت کردیم: امروز اجازه دهید در مورد جایگزینی رادیکال آزاد صحبت کنیم و برش (شکاف اکسیداتیو) را برای آخر رها کنیم.
همانطور که در مورد همه چیز در این سریال گفتم، نکته این است که درک نکنید چرا هنوز، اما بتوانیم از روی نمودارها ببینیم که چه پیوندهایی شکسته و تشکیل شده اند. شما باید نحوه خواندن نمودارهای خطی و همچنین مفهوم ایزومرها را بدانید. اما به غیر از آن هیچ مهارت بیشتری لازم نیست. نکته اینجاست که بتوانی طرح را دنبال کنید – دیدن چی اتفاق می افتد. سری پست های بعدی به جزئیات بیشتری در مورد آن خواهد پرداخت چرا اتفاقات رخ می دهد
بیایید دو مثال واقعا ساده بیاوریم. اگر یک هیدروکربن ساده مانند اتان (CH3CH3) بگیرید و آن را با گاز کلر (Cl2) در تاریکی نگه دارید، مطلقاً هیچ اتفاقی نمی افتد.

اما وقتی کاور را باز می کنید و اجازه می دهید نور به داخل بتابد، اتفاق جالبی می افتد. همانطور که در اولین مثال زیر مشاهده می شود، یکی از هیدروژن های موجود در اتان با یک اتم کلر جایگزین می شود و CH3CH2Cl (اتیل کلرید) را تشکیل می دهد. در طول مسیر، ما همچنین یک معادل اسید هیدروکلریک (HCl) تشکیل می دهیم. به عبارت دیگر، ما در حال شکستن CH و تشکیل C-Cl هستیم. (چرا ممکن است این اتفاق بیفتد؟ فعلاً در مورد آن صحبت نمی کنم. اما فراموش نکنید که نور (فوتون ها) حامل انرژی هستند و این انرژی می تواند برای شکستن انواع خاصی از پیوندها کافی باشد.)
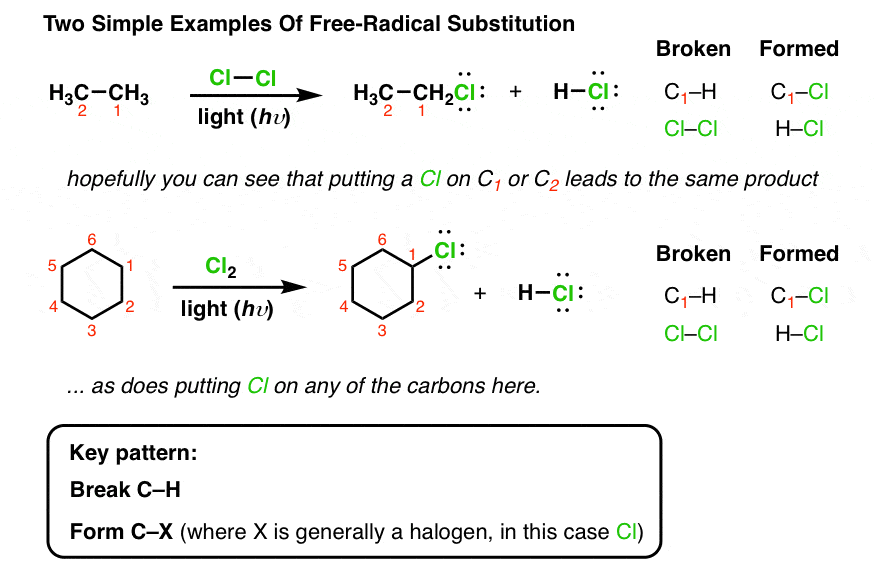
اگر به خاطر داشته باشید، این بسیار شبیه به الگویی است که قبلاً برای واکنشهای جایگزینی دیدیم: جایگزینی یک گروه در کربن با گروه دیگر. چیزی که این جایگزینی را با مثال قبلی متفاوت می کند، این واقعیت است که ما به نور یا نوع دیگری از آغازگر نیاز داریم تا واکنش رخ دهد. این قطعاً در مورد نمونه های موجود در اولین پست تعویض صدق نمی کند. (اسپویلر – نام «جایگزینی رادیکال آزاد» مسیر پیشنهادی برای انجام این جایگزینی را به ما می گوید، اما در حال حاضر می توانید آن را به عنوان «جایگزینی وابسته به نور» در نظر بگیرید.)
واکنش دوم مثال دیگری را نشان می دهد: تیمار سیکلوهگزان با Cl2 (1 معادل) سیکلوهگزیل کلرید و HCl می دهد. همان الگوی ضروری: CH را بشکنید، C-Cl را تشکیل دهید. این واکنش همچنین به وجود نور وابسته است (همانطور که همه واکنش های زیر خواهد بود).
ممکن است متوجه شوید که جایگزینی اتان یا سیکلوهگزان با کلر می تواند تنها به یک محصول ممکن منجر شود. بنابراین چه اتفاقی می افتد اگر از چیزی کمی متفاوت استفاده کنید – مثلاً بوتان؟ بیایید نگاه کنیم:
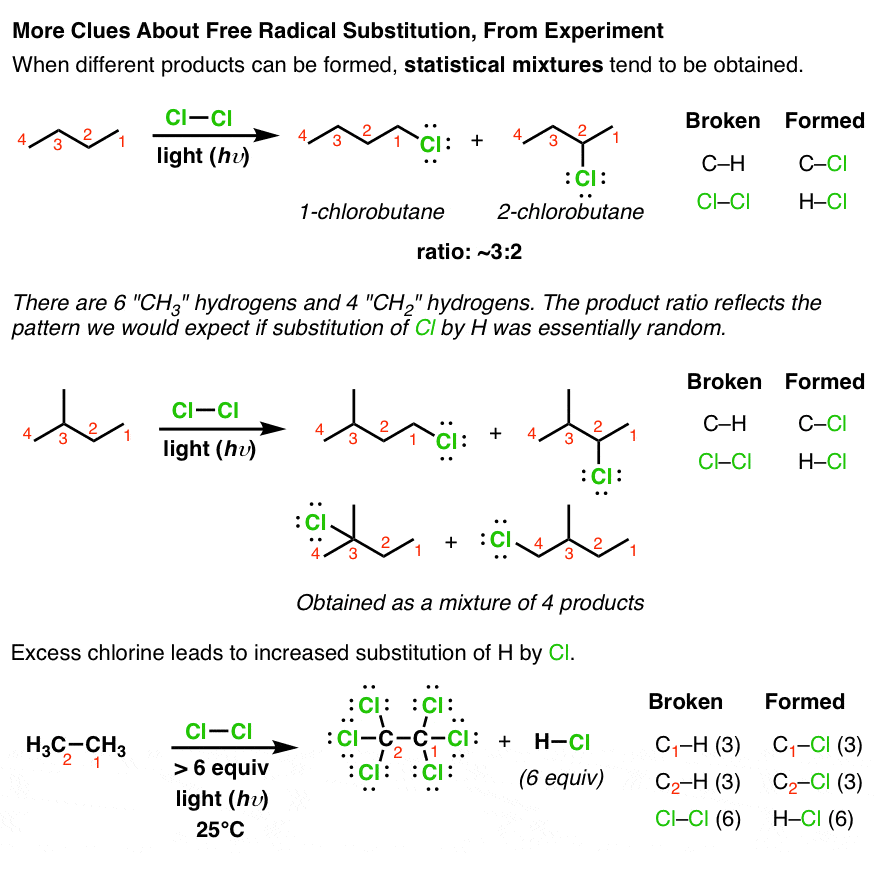
ببینید که ما دو محصول ممکن داریم – 1-کلروبوتان و 2-کلروبوتان- و آنها در نسبت 3:2 تشکیل شده اند. تصادفی نیست، این نیز نسبت هیدروژن های CH3 (6 عدد وجود دارد) به هیدروژن های CH2 (4) است. بنابراین در اصل، جایگزینی بوتان تقریباً تصادفی است. اگر از آلکان پیچیده تری مانند 2-متیل بوتان استفاده کنیم، این نیز صادق است.
دوباره توجه داشته باشید که ما همیشه همین واکنش را انجام می دهیم: یک پیوند CH را بشکنید، یک پیوند C-Cl تشکیل دهید. همان الگو مواد اولیه مختلف، محصول متفاوت، اما همان الگو
اگر مقدار زیادی گاز کلر استفاده کنید چه اتفاقی می افتد؟ خوب، مانند مثال سوم شروع به جایگزینی تمام هیدروژن های هیدروکربن می کند. این همان واکنش (جایگزینی) است که فقط چندین بار تکرار شده است. اینجا هیچ چیز جدیدی نیست، در واقع!
به هر حال: ما از تئوری برای پیش بینی این نتایج استفاده نمی کنیم، اینها نتایجی هستند که آزمایش ها به ما می گویند. هیچ کس از قبل این نتایج را پیش بینی نکرده بود. آنها فقط آزمایش ها را انجام دادند و این نتایج است. این شیمی آلی است. این نظریه پس از آن به وجود می آید که ما به اندازه کافی نتایج تجربی برای شروع فرضیه سازی داشتیم.
آخرین اسلاید کلر تنها هالوژن جدول تناوبی نیست. فلوئور (F2)، برم (Br2) و ید (I2) چطور؟
بیایید به برم و ید نگاه کنیم. فلوئور را تا آخر می گذاریم.
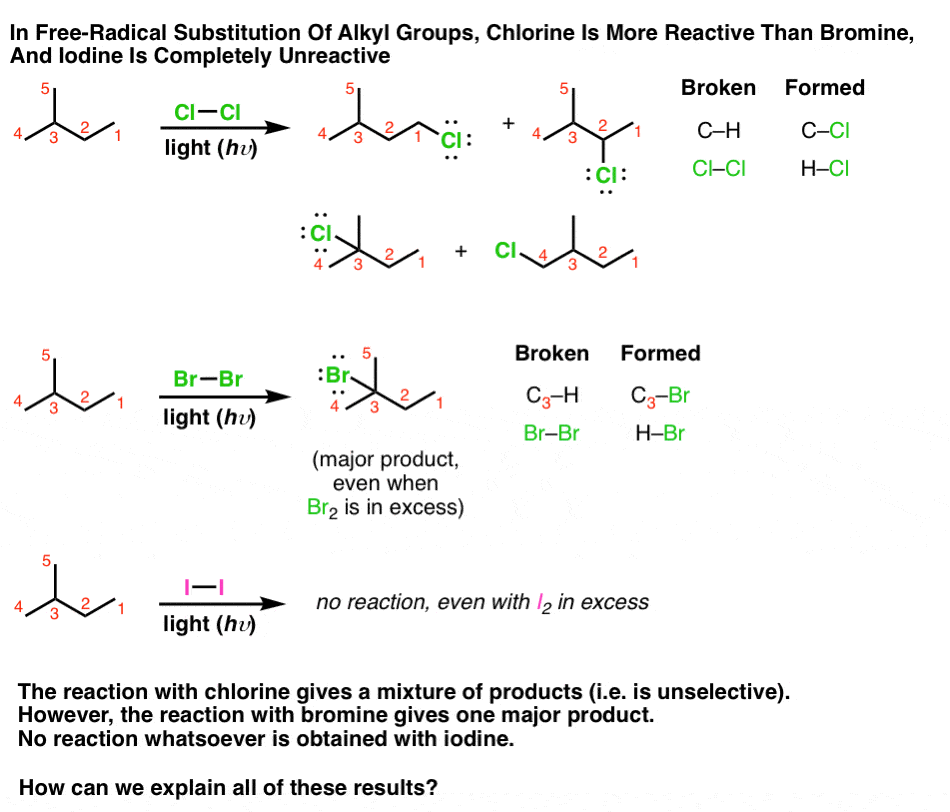
برم خنک است. وقتی 2-متیل بوتان را می گیریم و آن را با برم درمان می کنیم، یک محصول عمده به دست می آوریم: 2-برومو-2-متیل بوتان. این محصول اصلی است حتی اگر مقدار زیادی Br2 اضافه کنیم. این یک ویژگی مفید است.
ید چطور؟ خوب، همانطور که می بینید، کار زیادی انجام نمی دهد. مهم نیست که چه مقدار معادل ید اضافه می کنید یا چه مقدار نور – هیچ اتفاقی نمی افتد. جالب هست!
پس چگونه می توانیم همه این نتایج را توضیح دهیم؟ چگونه میتوانیم برای توضیح همه این مشاهدات تجربی مختلف، به فرضیههایی دست پیدا کنیم؟
PS.OK، باشه. من به فلورین اشاره نکردم. چرا هنوز در مورد فلوئور صحبت نکرده ایم؟ از آنجا که گاز فلوئور، گورکن عسل شیمی است. واقعا به درد نمیخوره با هر چیزی که در مقابل آن قرار دهید واکنش نشان می دهد، و مگر اینکه 1) از نظر فنی بسیار صلاحیت داشته باشید، 2) از ایمنی بسیار آگاه باشید، و 3) کمی دیوانه کننده، گاز فلوئور چیزی است که هرگز و هرگز نباید با آن کار کنید.
[youtube]http://www.youtube.com/watch?v=vtWp45Eewtw[/youtube]
پست بعدی در سری: مقدمه ای بر واکنش های برش اکسیداتیو
