فرمالیسم حالت اکسیداسیون
در پایان Gen Chem، محاسبه حالت اکسیداسیون فلزات مختلف باید کاملاً آشنا باشد.
این چیزی است که شما انجام می دهید. یک ترکیب معمولی – FeCl را بگیرید3، برای مثال. با هر پیوندی که بین فلز و اتم دیگری وجود دارد طوری رفتار کنید که انگار یک پیوند یونی است. این بدان معناست که عناصر الکترونگاتیو بیشتر (مثلاً کلر یا اکسیژن) بارهای منفی را تحمل می کنند و عنصر الکترونگاتیو کمتر (مانند فلز) بار مثبت را تحمل می کند.
اگر ترکیب خنثی باشد، مجموع حالت های اکسیداسیون نیز باید خنثی باشد. (اگر ترکیب دارای بار باشد، حالت های اکسیداسیون را مطابق با آن تنظیم می کنید تا مجموع آنها برابر با بار باشد).
1. محاسبه حالات اکسیداسیون در ترکیبات معدنی

حالا این یک تمرین سرگرم کننده است. سعی کنید همان قوانین را در مورد کربن اعمال کنید.
کمی احساس عجیبی خواهد داشت. چرا؟ زیرا دو تفاوت اساسی وجود دارد.
- اولینکربن اغلب الکترونگاتیوتر است (2.5) نسبت به برخی از اتمهایی که به آنها متصل است (مانند H, 2.2). پس در این مورد چه می کنید؟
- ثانیاً برخلاف پیوندهای فلز-فلز، پیوندهای کربن-کربن در همه جا وجود دارند. پس چگونه با آنها برخورد می کنید؟
دو جواب
- در یک پیوند CH، H به گونه ای رفتار می شود که گویی حالت اکسیداسیون 1+ دارد. این بدان معنی است که هر پیوند CH حالت اکسیداسیون کربن را 1 کاهش می دهد.
- هر دو پیوند بین یک اتم روی حالت اکسیداسیون تأثیر نمی گذارد (به یاد بیاورید که حالت اکسیداسیون Cl در Cl-Cl (و H در HH) صفر است. بنابراین یک کربن متصل به 4 کربن حالت اکسیداسیون صفر دارد.
بنابراین بر خلاف فلزات، که تقریبا همیشه در حالت اکسیداسیون مثبت هستند، حالت اکسیداسیون کربن می تواند به طور گسترده ای متفاوت باشد، از -4 (در CH4) به +4 (مانند CO2). در اینجا چند نمونه آورده شده است.
2. محاسبه حالت اکسیداسیون کربن
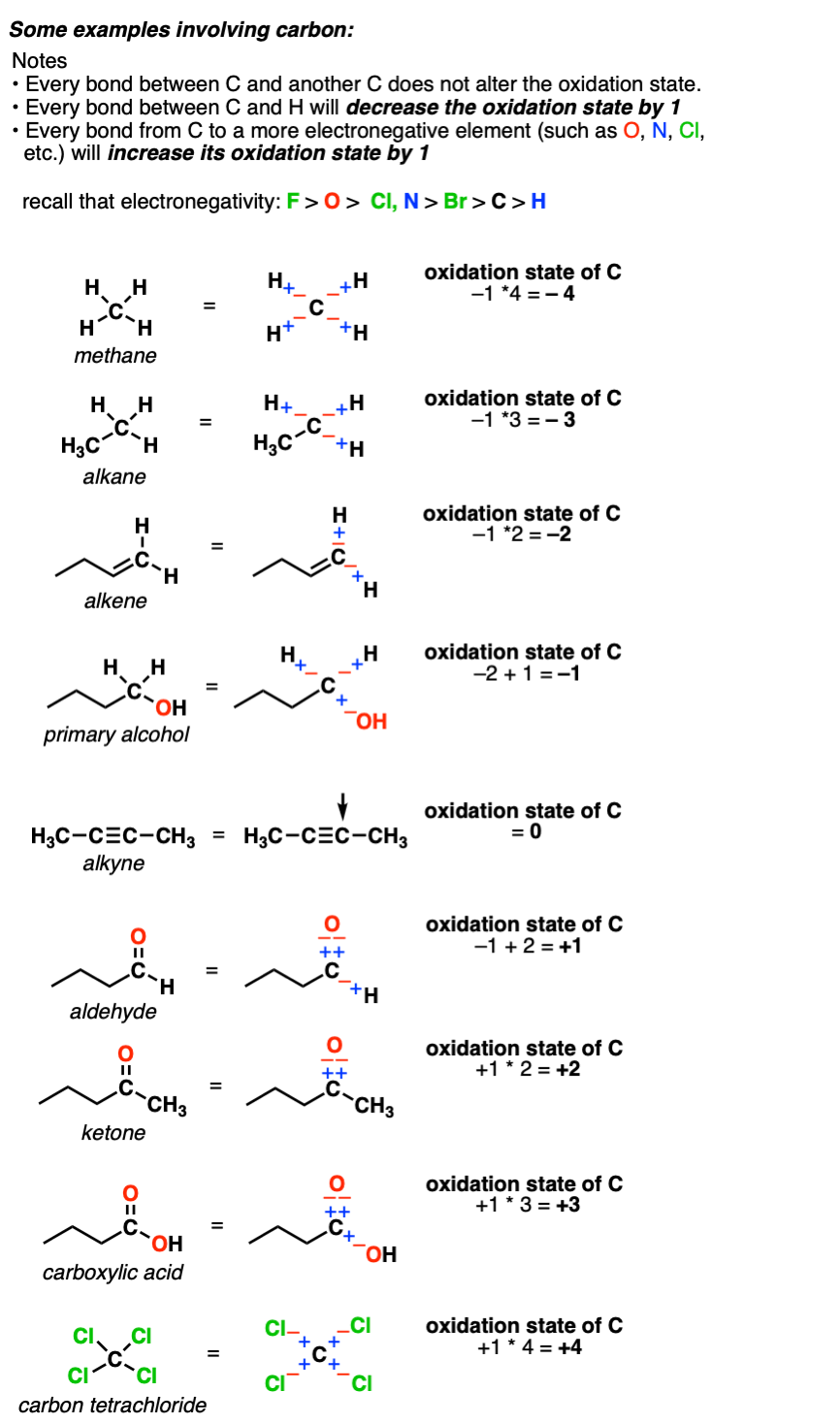
(فراموش نکنید که به دلایلی به این “فرمالیسم” می گویند. شارژ کربن نیست واقعا +4 یا -4. اما فرمالیسم حالت اکسیداسیون به ما کمک میکند تا مسیر حرکت الکترونها را پیگیری کنیم، که خیلی زود به کار خواهد آمد.
با درک نحوه محاسبه حالات اکسیداسیون کربن، ما برای مرحله بعدی آماده هستیم: درک تغییر می کند در حالت اکسیداسیون در کربن، از طریق واکنش هایی به نام اکسیداسیون ها (که در آن حالت اکسیداسیون افزایش می یابد) و کاهش می دهد (که در آن حالت اکسیداسیون کاهش می یابد). دفعه بعد بیشتر در مورد آن.
