مقدمه ای بر واکنش های جانشینی هسته دوست
امروز مجموعه جدیدی از پستها در مورد قدم زدن در یکی از کلاسهای کلیدی واکنش در شیمی آلی آغاز میشود: واکنشهای جایگزینی. هدف این مجموعه این است که به شما بیاموزد چگونه واکنشهای جانشینی را زمانی که به شما ارائه میشوند تشخیص دهید و انواع مختلف واکنشهای جایگزینی و مکانیسمهای آنها را شناسایی کنید.
اما امروز، بیایید فقط «واکنشهای جایگزین» را معرفی کنیم.
فهرست مطالب
- الگوی کلیدی در یک واکنش جایگزینی شکستن و تشکیل یک پیوند جدید در کربن است
- دو شریک واکنشی در یک واکنش جانشینی یک “هسته دوست” غنی از الکترون و یک “الکتروفیل” فقیر از الکترون هستند.
- واکنشهای جانشینی شبیه واکنشهای اسید-باز هستند، با این تفاوت که به جای H+، یک پیوند تشکیل میشود و در کربن میشکند.
- چهار جزء یک واکنش جانشینی عبارتند از: هسته دوست، الکتروفیل، محصول و گروه ترک
- یادداشت
1. الگوی کلیدی در واکنش جانشینی شکستن و تشکیل یک پیوند جدید در کربن است.
واکنشهای جایگزینی یکی از متنوعترین و مهمترین واکنشها در تمام شیمی آلی هستند. در زیر سه نمونه از این واکنش ها ترسیم شده است.*
با فرض اینکه هیچ دانش پس زمینه ای به جز درک واکنش های باز اسیدی و دانش در مورد چگونگی دیدن هیدروژن های پنهان وجود ندارد، به دقت نگاه کنید: در هر مورد چه پیوندهایی تشکیل و شکسته می شوند؟
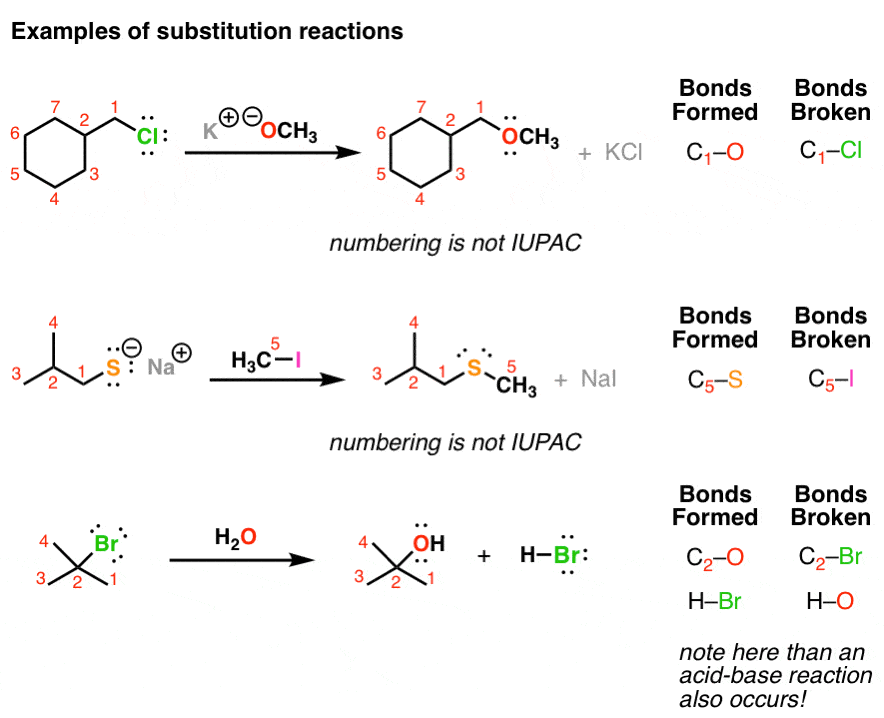
در هر مورد ما هستیم شکستن پیوند در کربن و تشکیل پیوند جدید در کربن. به عبارت دیگر کربن شرکای خود را عوض کرده است.
بیایید اولین واکنش را در نظر بگیریم و سوال کلیدی دوم را هنگام درک یک واکنش جدید بپرسیم: الکترون ها در مواد اولیه ما کجا هستند؟
2. دو شریک واکنشی در یک واکنش جانشینی یک “هسته دوست” غنی از الکترون و یک “الکتروفیل” فقیر از الکترون هستند.
ما یک گونه غنی از الکترون داریم ( اکسیژن) ایجاد پیوند با گونه های فقیر از الکترون (کربن متصل به کلر). با استفاده از الکترونگاتیوهای نسبی برای درک واکنش پذیری و دانستن اینکه بارهای مخالف جذب می شوند و الکترون ها از منفی به مثبت جریان می یابند، تصور برهمکنش بین این دو اتم آسان است.
![]()
سوال سوم: این الکترون ها چگونه حرکت می کنند، سپس؟
خوب، اکسیژن از بار منفی به خنثی رسید – از داشتن یک جفت الکترون به اشتراک گذاری یک جفت الکترون با کربن و کلر از خنثی به بار منفی تبدیل شد – از اشتراک یک جفت الکترون با کربن تا داشتن یک جفت الکترون.
خیلی زود است که به طور قطعی بگوییم چگونه این واکنش در این مرحله بدون نتایج تجربی بیشتر رخ می دهد، اما هر توضیحی در مورد چگونگی شکل گیری و شکستن پیوندها (مکانیسم) باید زمان تشکیل پیوند OC و شکستن پیوند C-Cl را توضیح دهد.
3. واکنشهای جانشینی شبیه واکنشهای اسید-باز هستند، با این تفاوت که در کربن به جای H+ یک پیوند تشکیل میشود و میشکند.
به هر حال، آیا این نوع واکنش شما را به یاد چیزی می اندازد که قبلا دیده اید؟ باید، اگر فقط کمی. این است یک جور هایی مانند یک واکنش اسید-باز، که در آن ما در حال شکستن و تشکیل یک پیوند جدید در هیدروژن هستیم، با این تفاوت که در عوض در حال شکستن و تشکیل یک پیوند روی کربن هستیم.
بیایید به 4 جزء واکنش اسید باز نگاه کنیم. ما یک گونه غنی از الکترون (یک باز) داشتیم که یک جفت الکترون را به گونه ای فقیر از الکترون (هیدروژن) اهدا می کرد، که یک اسید مزدوج (پایه به اضافه پروتون) و یک باز مزدوج (قسمتی که با از دست دادن اسید شروع شد شروع شد). پروتون)
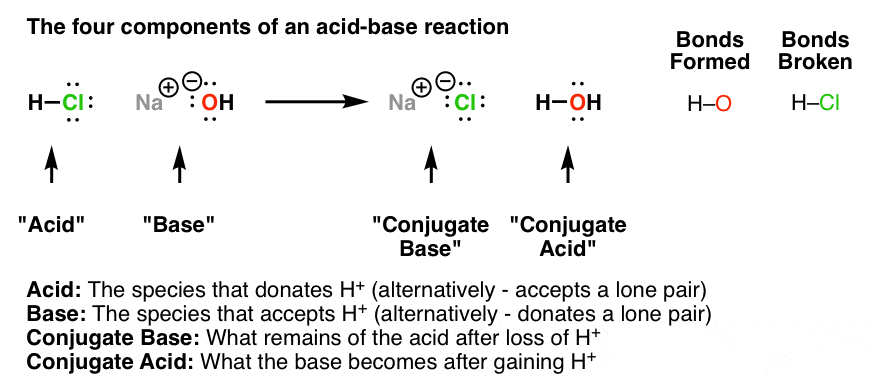
4. چهار جزء یک واکنش جانشینی عبارتند از: هسته دوست، الکتروفیل، محصول، و گروه ترک
اصطلاحات متفاوتی برای توصیف هر یک از این اجزا برای یک واکنش جایگزینی، بر خلاف واکنشهای باز اسیدی ایجاد شده است.
در واکنش جانشینی، ما یک گونه غنی از الکترون (اکسیژن) داریم که یک جفت الکترون به گونه فقیر از الکترون (کربن) اهدا می کند که یک محصول جدید (الکل) و یک پایه جدید (قسمتی که در زمان شروع به کار می کند) تشکیل می دهد. پیوند C-Cl شکست).
را هسته دوست گونه ای غنی از الکترون است که یک جفت الکترون به کربن اهدا می کند.
را الکتروفیل (یا “سوبسترا” یا “آلکیل هالید” در این مورد) گونه ای است که جفت الکترون را می پذیرد.
گونه تشکیل شده است تولید – محصول.
پایه جدیدی که از کربن جدا می شود، نامیده می شود ترک گروه
برای این واکنش همه را کنار هم قرار دهید:
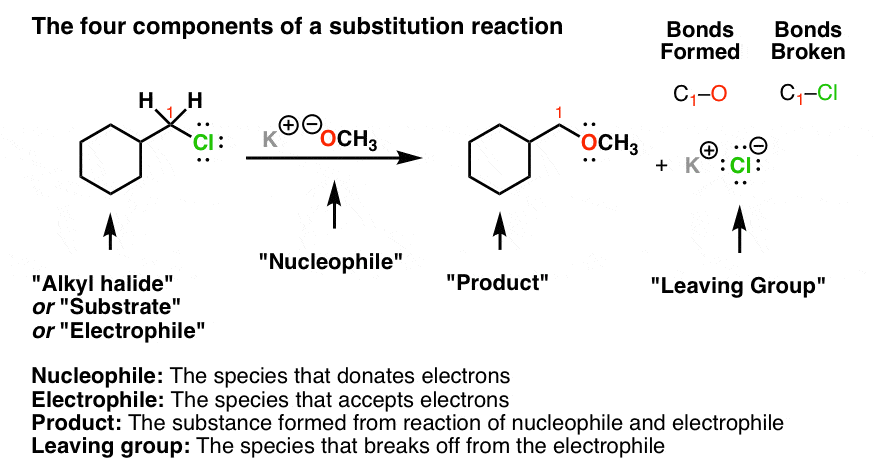
دفعه بعد، بیایید این مفهوم جدید – “هسته دوستی” را با جزئیات بیشتر درک کنیم، و اینکه چگونه با پایه تفاوت دارد.
پست بعدی: هسته دوست ها و الکتروفیل ها
یادداشت
یادداشت 1. شیمی یک علم تجربی است. برخلاف قضایای مثلاً ریاضیات، که میتوان از مجموعهای از مقدمات اولیه استخراج کرد، مجموعه دانش در علم شیمی دانشی است که از طریق آزمایشها و مشاهدات به دست آمده است. ما فقط با نگاه کردن به عقب از نتایج آزمایشهایمان، مقدمات را درمییابیم!
نکته اصلی اینجاست که مشاهده میشود که واکنشهایی که در اینجا توضیح داده میشوند رخ میدهند، و این مشاهدات هزاران بار تکرار شدهاند توسط دانشمندانی که در دهههای مختلف کار میکنند، از کشورهای مختلف، که به بسیاری از زبانهای مادری صحبت میکنند. این چیزها فقط کار می کند. برخی از آنها را ممکن است در یک آزمایشگاه آموزشی انجام دهید. دیگران، شما فقط باید حرف ما را قبول کنید (اما همیشه آزاد هستید که سعی کنید این مشاهدات را جعل کنید). شاید روزی این فرصت را پیدا کنید که برخی از آنها را خودتان انجام دهید.
