ایزومرهای ساختاری پروپان (عالی هستند)
در این پست، ترکیبهای مختلف پروپان را بررسی میکنیم و خواهیم دید که به دلیل یک تعامل فضایی جدید، مانع چرخش کمی بالاتر از اتان است. ما طرح نیومن پروپان را از منظرهای متعدد ترسیم می کنیم، برآمدگی های مختلف نیومن را در حین چرخش 360 درجه نشان می دهیم و نمودار انرژی در مقابل زاویه دو وجهی را ترسیم می کنیم!
فهرست مطالب
- خلاصه: مبهم، گرفتگی، برآمدگی های نیومن، زاویه دو وجهی.
- پروپان چطور؟
- تبدیل پروپان به پروجکشن نیومن
- نقش چشم انداز: تجزیه و تحلیل یک پیوند در یک زمان
- فعل و انفعالات گرفتگی در پروپان
- تجسم سد چرخشی در پروپان
- خلاصه
- یادداشت
- خودت امتحان کن
- (پیشرفته) مراجع و مطالعه بیشتر
1. خلاصه: تلو تلو خورده، گرفتگی، برآمدگی های نیومن، زاویه دو وجهی
در پست قبلی [see: Staggered vs Eclipsed Conformations of Ethane] دیدیم که اتان دو تا دارد مهم ایزومرهای ساختاری، بسته به جهت گیری دو گروه متیل در امتداد پیوند C-C.
- در گرفت ترکیب، هیدروژنهای روی بلوک کربن جلو (یا «کسوف») هیدروژنهای کربن پشتی وقتی مستقیماً در امتداد پیوند CC نگاه میکنیم، مانند دو نماد مرسدس بنز که روی هم قرار گرفتهاند.
- در مبهوت ترکیب، هیدروژن های موجود در کربن جلو دو نیم کن هیدروژن های موجود در کربن پشتی، به طوری که اگر در امتداد پیوند C-C نگاه کنیم، هیدروژن ها همه 60 درجه از یکدیگر فاصله دارند.
- دیدیم که طرح ریزی نیومن یک کمک بصری مفید برای تجسم ساختارهای گرفتگی و مبهم و همچنین چرخش پیوند است.
- ما هم تعریف کردیم زاویه دو وجهی به عنوان زاویه بین یک انتخاب دلخواه جایگزین فردی در جلو کربن و یک شخصی جایگزین در پشت کربن وقتی به دنبال پیوند کربن-کربن هستید. یک تشبیه مفید برای زاویه دو وجهی، زاویه بین عقربه ساعت و دقیقه عقربه در صفحه ساعت است، که در آن زاویه دو وجهی 0 درجه در ساعت 12:00، 60 درجه در ساعت 2:00، 120 درجه در ساعت 4:00 و غیره است. .
- هنگامی که دو جایگزین دارای زاویه دو وجهی -90 ° ≤ 0 ° ≤ + 90 باشند. syn. وقتی زاویه دو وجهی 90+ ≤ 180 درجه ≤ -90 درجه داشته باشند. ضد
- ایزومرهای ساختاری می توانند از نظر انرژی متفاوت است; در اتان sترکیب برچسبگذاری شده پایدارتر از ترکیب گرفت شده است با 3.0 کیلوکالری در مول که به حدود 1.0 کیلوکالری در مول در هر برهم کنش HH گرفتار می رسد. یکی از راههای فکر کردن به این موضوع، دافعههای بین هیدروژنها (یا به عبارت دقیقتر ابرهای الکترونی آنها) است. راه های دیگری نیز برای فکر کردن در مورد آن وجود دارد.
2. ایزومرهای ساختاری پروپان
اکنون که به اتان نگاه کردیم، به سراغ آلکان بالاتر بعدی برویم: پروپان.
رسم پروپان به صورت نمودار خطی ساده است. درست مانند شکلهای چوبی افراد که جزئیات دانهای مانند انگشتان دست و پا را حذف میکنند، نمودارهای خطی مولکولها محل قرارگیری هیدروژنها را حذف میکنند.
در بیشتر مواقع مشکلی نیست، اما اگر میخواهیم در مورد ترکیبها بحث کنیم، باید نمودار خطی پروپان را گسترش دهیم تا نشان دهیم هیدروژنها کجا هستند.
بدیهی است که اولین کار این است که مطمئن شوید که هیدروژن ها به شکل چهار وجهی مناسبی در اطراف هر کربن قرار گرفته اند. (بله، ممکن است این مشکل را خراب کنید، همانطور که آکادمی خان گاهی اوقات انجام می دهد [see post: Common Mistakes: Drawing Tetrahedral Carbons] )
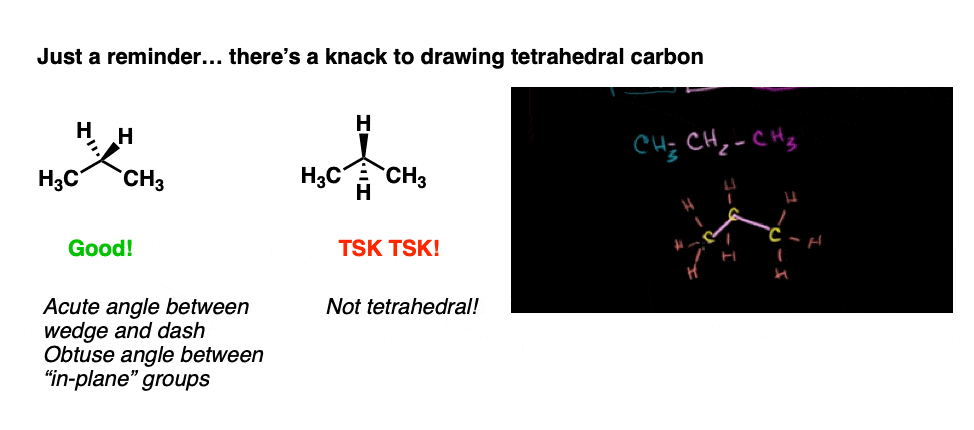
دو جایگزین را در صفحه صفحه، با یک گوه و یک خط تیره و یک نگه دارید حاد زاویه (<90 درجه) بین گوه و خط تیره.
در اینجا یک نقاشی از پروپان است که تمام هیدروژن ها را نشان می دهد. من خودسرانه کربن سمت چپ را به صورت C-1 شماره گذاری کرده ام.
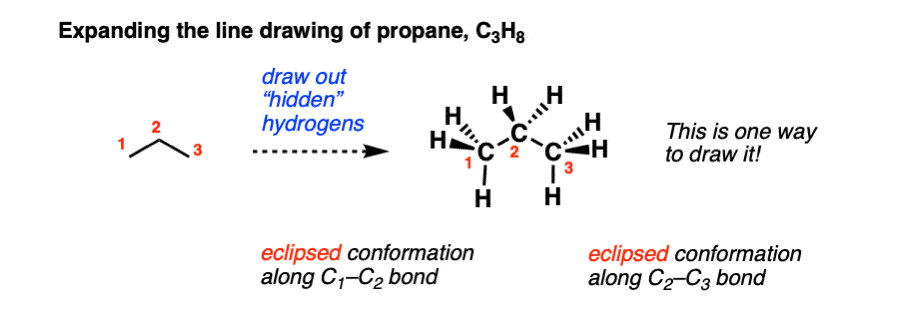
در گسترش هیدروژن های موجود در هر کربن، اکنون با جزئیات مزاحم ایزومریسم ساختاری روبرو می شویم!
در شکل بالا، وقتی پروپان را منبسط کردم، ترسیم یک را انتخاب کردم گرفت ترکیب در امتداد هر دو پیوند C1-C2 و C2-C3. این یکی از راههای انجام آن است و همینطور است اشتباه نیست (حتی اگر انرژی بیشتری داشته باشد).
با این حال، راه های دیگری نیز برای بیرون کشیدن پروپان وجود دارد. من به همان خوبی می توانستم کربن C1-C2 را بکشم مبهوت و C2-C3 به عنوان گرفت (زیر) یا C1-C2 و C2-C3 به عنوان هر دو مبهوت.
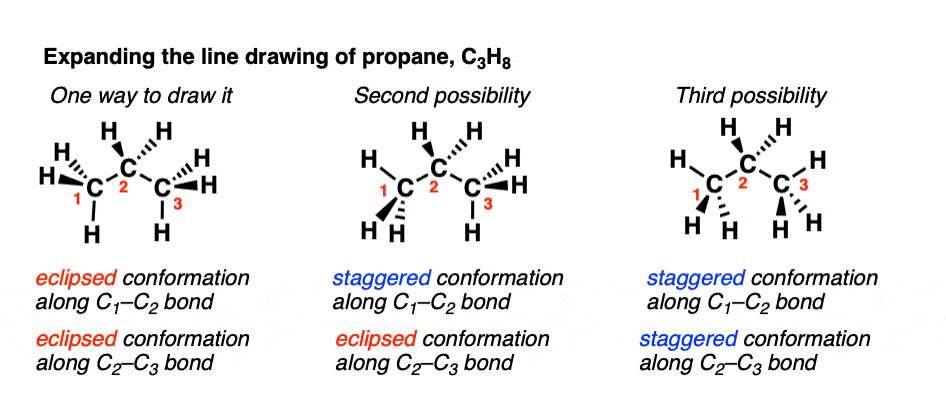
(البته ترکیبات دیگری نیز وجود دارد که می توان ترسیم کرد – یک عدد بی نهایت، اما از آنجایی که آنها حداقل یا حداکثر انرژی نیستند، معمولاً برای ما جالب نیستند. 3600 ثانیه در یک ساعت وجود دارد، اما آخرین باری که کسی به جای ساعت 8 ساعت 7:46:23 از شما خواسته است که شما را ملاقات کند، کی بوده است؟)
این واقعا مهم نیست هم تا چه اندازه پروپان را در چه ترکیبی به تصویر می کشیم. از آنجایی که وجود دارد چرخش آزاد در مورد پیوندهای C1-C2 و C2-C3، تمام انطباق ها هستند قابل تبدیل.
از طریق GIPHY
در پروپان، ترکیب کم انرژی، ترکیبی است که همه کربن ها در آن قرار دارند مبهوت نسبت به یکدیگر (بالا سمت راست).
گفت: آیا راه سادهتر و شهودیتری برای تحلیل این ترکیبها وجود دارد؟ آره!
3. تبدیل پروپان به نیومن پروجکشن
بهترین راه برای تجزیه و تحلیل جهت گیری در امتداد پیوند کربن-کربن استفاده از a است طرح ریزی نیومن.
اولین قدم در طراحی نیومن این است که یک چشم انداز را انتخاب کنید
در اولین ترسیم پروپان، بیایید انتخاب کنیم که در امتداد پیوند C1-C2، مانند این نگاه کنیم:
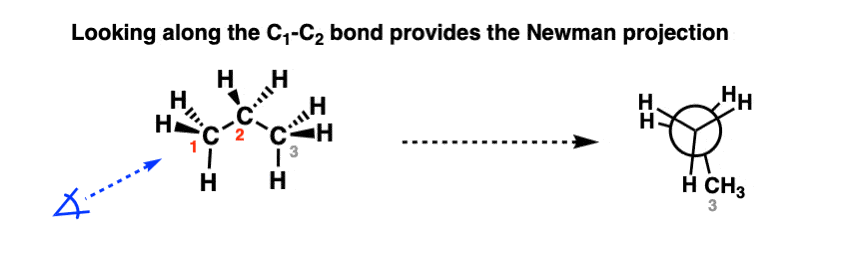
چگونه به این طرح نیومن رسیدیم؟ با نگاه کردن در امتداد پیوند C1-C2، مانند زیر:
از طریق GIPHY
4. نقش چشم انداز: تجزیه و تحلیل یک پیوند در یک زمان
در نهایت، فرافکنی نیومن فقط یک است ترسیم پرسپکتیو یک جسم سه بعدی؛ یک مولکول
در حالی که هنرمندان و عکاسان باید برای انتخاب پرسپکتیو مناسب برای ترسیم افراد یا ساختمان ها فکر زیادی کنند، وظیفه ما بسیار ساده تر است زیرا برای طرح ریزی نیومن، ما باید به طور مستقیم در امتداد یک پیوند نگاه کنید.
در زیر، من پروپان را طوری ترسیم کردم که یک وجود دارد گرفت ترکیب در امتداد پیوند C1-C2 و a مبهوت ترکیب در امتداد پیوند C2-C3.
هنگام ترسیم نیومن باید مشخص کنیم که پیوندی که ما به دنبال آن هستیم و در چه جهتی.
این به این دلیل است که حتی در یک مولکول ساده مانند پروپان، 4 روش مختلف وجود دارد که ما میتوانیم در امتداد پیوندهای CC نگاه کنیم، و بنابراین 4 پیشبینی مختلف نیومن فقط برای این ترکیب وجود دارد!
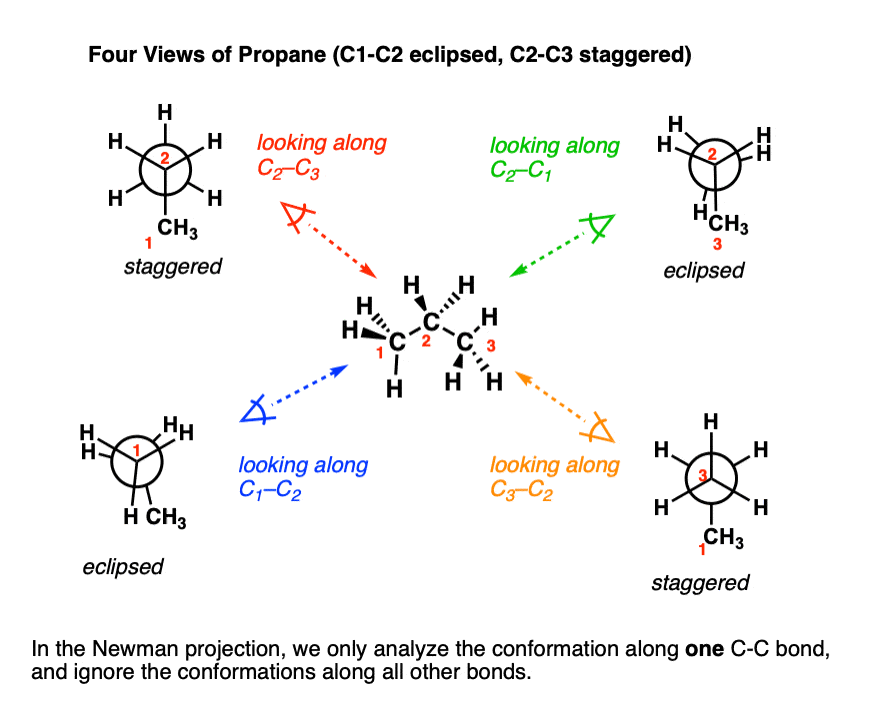
هیچ یک از این دیدگاهها «اشتباه» نیستند، درست مانند اینکه هیچ دیدگاه «اشتباهی» برای ترسیم خانه وجود ندارد. اما هر چشم انداز جنبه های مختلفی از ساختار مولکول را نشان می دهد.
نکته مهمی که باید به آن توجه کرد این است ما یک پیوند کربن-کربن را در یک زمان تجزیه و تحلیل می کنیم و چشم پوشی ترکیبات در امتداد سایر پیوندها
بنابراین در طرح نیومن برای نگاه کردن در امتداد C1-C2، ما فقط C3 را به عنوان “CH” ترسیم می کنیم3” بدون در نظر گرفتن در مورد اینکه آیا آن را تحت الشعاع قرار می دهد یا مبهوت نسبت به C2.
وقتی نیومن را برای نگاه کردن در امتداد C2-C3 رسم می کنیم، C1 را به صورت “CH” رسم می کنیم3“، مهم نیست چه. یک پیوند در یک زمان.
[Breaking down a big problem into a lot of tiny problems, solving them in isolation, and then building them back up to get the big picture (“reductionism”) is a powerful problem-solving technique in organic chemistry. By analyzing the conformations in a tiny molecule like propane, we can then apply what we’ve learned to much bigger molecules. [Note 1] ]
5. فعل و انفعالات گرفتگی در پروپان
در پست قبلی به تجزیه و تحلیل ترکیبات اتان پرداختیم و دیدیم که شکل گرفتگی اتان حدود انرژی 3.0 کیلوکالری در مول بیشتر از ترکیب تلوتلو شده است.
که به یک برهمکنش HH تحت الشعاع تجزیه می شود که ارزشی در حدود 1.0 کیلوکالری در مول دارد.
سد چرخشی برای پروپان نیز اندازه گیری شده است. [Ref] 3.4 کیلوکالری در مول است.
چرا ممکن است مانع چرخشی برای پروپان بالاتر باشد؟ اینجاست که نگاه کردن به نیومن واقعا کمک می کند.
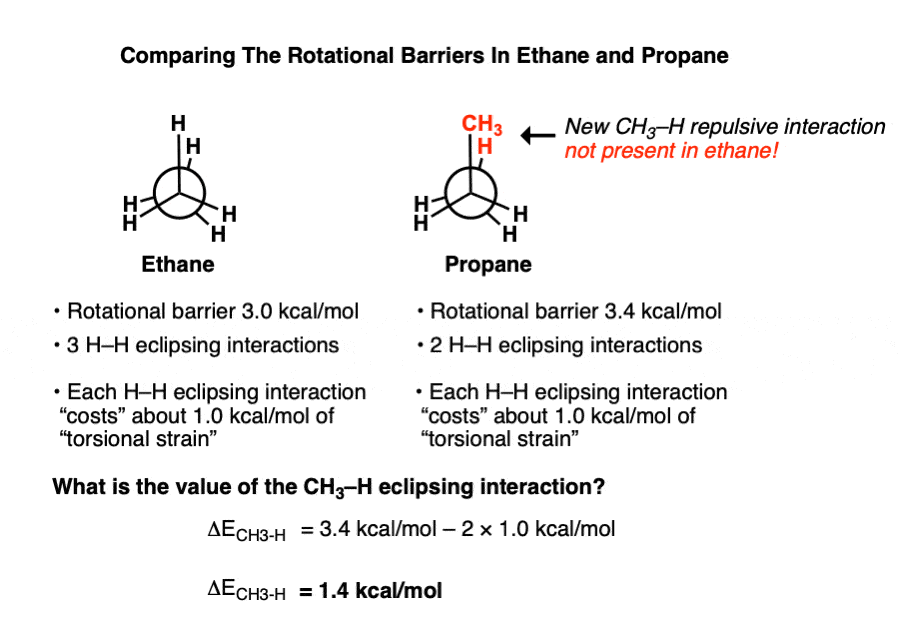
در پروپان یک CH وجود دارد3-برهمکنش دافعه H که در اتان وجود ندارد.
آنچه در اینجا اتفاق می افتد این است که CH3 گروه در مجاورت نسبتاً نزدیک با پیوند CH قرار دارد و ابرهای الکترونی اطراف هر گروه یکدیگر را دفع می کنند. این به عنوان دفع واندروالس شناخته می شود.
از آنجایی که CH3 بزرگتر از H است، ما انتظار داریم که این تعامل دافعه بسیار بزرگتر باشد.
اما چقدر بزرگتر؟
اگر فرض کنیم که هر یک از دو برهم کنش HH گرفتگی در پروپان 1.0 کیلوکالری در مول است، این مقدار CH را می دهد.3تعامل تحتالشعاع H به عنوان «هزینهیابی» 1.4 کیلو کالری در مول در انرژی کرنش
(به هر حال، این ارزش تقلیل گرایی است: ما می توانیم از مقدار 1.0 کیلوکالری در مول به ازای هر برهم کنش گرفتگی HH که از اتان گرفتیم استفاده کنیم و آن را به مولکول های بزرگتر با برهمکنش های HH گرفتگی اعمال کنیم).
به نظر می رسد که این مقدار 1.4 کیلو کالری در مول برای گرفتگی CH است3-H بسیار سازگار است، همانطور که در برخی مولکول های دیگر دیده می شود (برای یک برنامه، به Quiz Yourself مراجعه کنید! در زیر).
6. تجسم سد چرخشی در پروپان
در مرحله بعد، بیایید نگاهی دقیق تر به مشخصات انرژی سد چرخشی در پروپان داشته باشیم. ما با نگاه کردن به امتداد پیوند C2-C3 پروپان در شکل گرفت با گروه متیل C1 که مستقیماً به سمت بالا است نگاه می کنیم و زاویه دو وجهی خود را به عنوان زاویه بین گروه متیل و H که مستقیماً توسط آن گرفته می شود انتخاب می کنیم. از زاویه دو وجهی 0 درجه شروع می کنیم. در ویدیوی زیر هر کدام را به رنگ قرمز مشخص می کنیم.
اکنون، کربن پشتی (C3) را با افزایش 60 درجه میچرخانیم و انرژیها را در حین حرکت یادداشت میکنیم:
از طریق GIPHY
توجه داشته باشید که ترکیبات هر 120 درجه تکرار می شوند!
اگر واقعا مشتاق باشیم، حتی میتوانیم این انرژیها را ترسیم کنیم، که چیزی شبیه به این است.
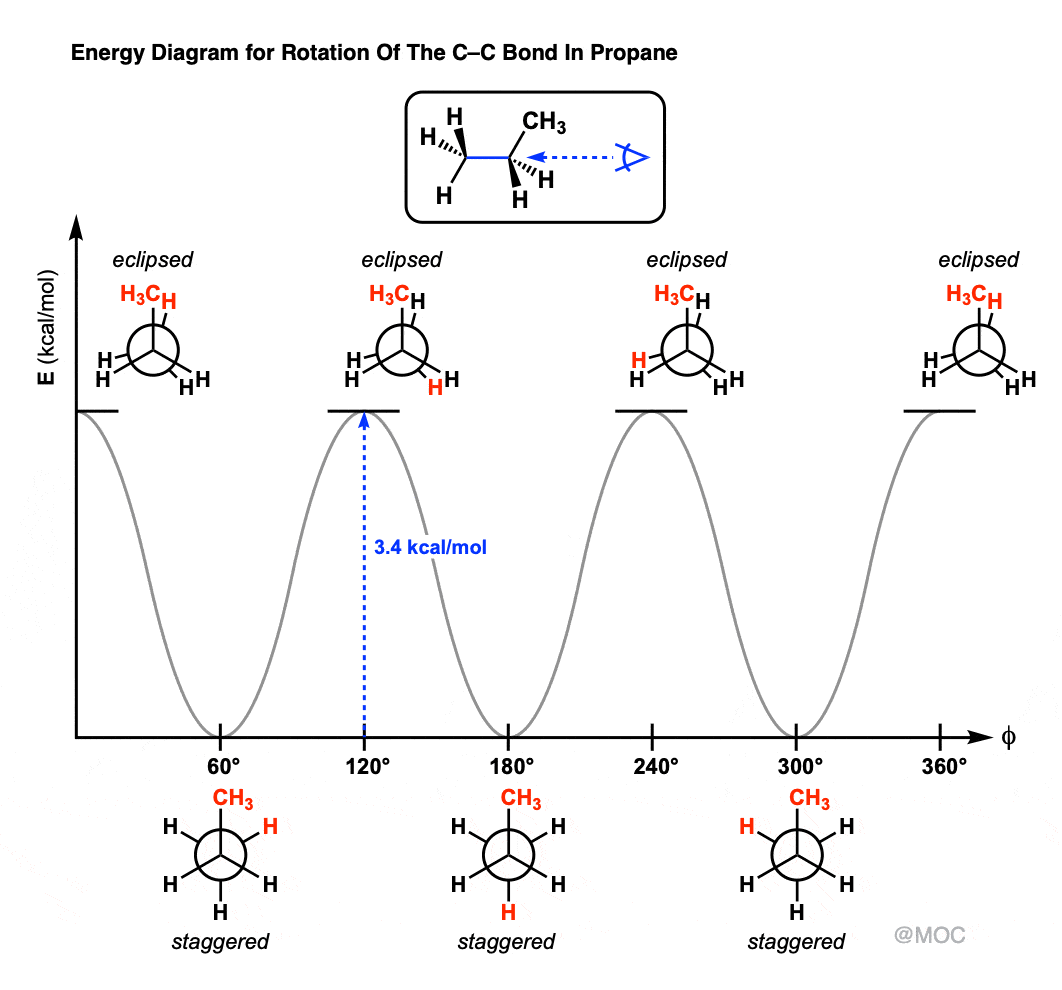
توجه داشته باشید که شکل این نمودار دقیقاً همان چیزی است که برای اتان دیدیم، با این تفاوت که مانع چرخشی بالاتر است.
(همیشه آنقدر ساده نخواهد بود، همانطور که در پست بعدی با بوتان خواهیم دید).
7. خلاصه: ایزومرهای ساختاری پروپان
تجزیه و تحلیل برای پیوند C2-C3 دقیقاً مشابه با پیوند C1-C2 است.
بنابراین، اکنون اطلاعات کافی برای محاسبه در اختیار داریم نسبت فامیلی پایداری سه ترکیب پروپان ترسیم شده در بالای پست.
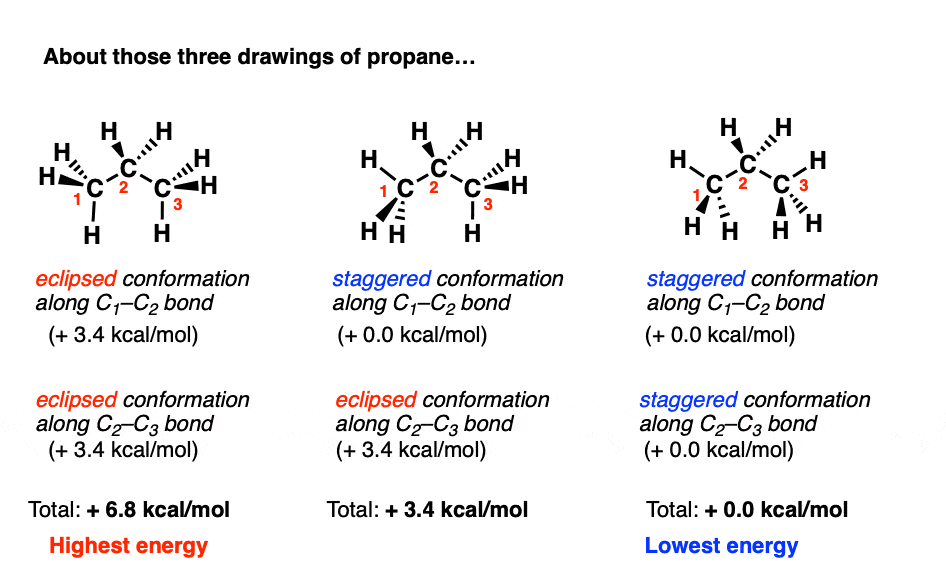
انرژی (مستقل، مبهم) حدود 6.8 کیلوکالری در مول نسبت به (کسوف، گرفتار) کمتر است.
به طور خلاصه:
- مانع چرخشی است 3.4 کیلو کالری در مول در پروپان در مقابل 3.0 کیلو کالری در مول در اتان که به دلیل 1.4 کیلو کالری در مول CH3-H تحت الشعاع تعامل. از آنجایی که CH3 از نظر اندازه بزرگتر از H است، ما باید انتظار داشته باشیم که وقتی گروه ها نزدیک به هم قرار دارند، مانند زمانی که آنها در کنار هم قرار دارند، شاهد دفع بیشتر وان دروالسی باشیم. syn.
- هنگام ترسیم طرح ریزی نیومن، منظرهای متعددی وجود دارد.
- هنگام ترسیم پروجکشن نیومن، ما بر روی انطباق تمرکز می کنیم یک باند CC در یک زمان، و همه انطباق های دیگر را نادیده بگیرید.
- نمودار انرژی دورانی پروپان a است موج سینوسی با سه ماکسیما، درست مثل اتان.
خیلی سرراست، امیدوارم. اما این فقط یک گرم کردن برای عمل اصلی است.
در پست بعدی به بررسی ترکیبات می پردازیم بوتان، که دارای دو نوع جدید تعامل فضایی است که قبلاً ندیده ایم!
یادداشت
یادداشت 1. ساختارها در طبیعت بسیار مهم هستند – برای مثال، شکل سه بعدی پروتئین ها تحت تأثیر چرخش صدها یا هزاران پیوند قرار می گیرد و کشف انرژی این ترکیب ها به ما کمک می کند تا درمان های بهتری طراحی کنیم. پیشرفت های مهم در نحوه محاسبه این انرژی ها مبنایی برای جایزه نوبل شیمی 2013 بود.
با تشکر از جرمی ترن برای کمک به نمودار انرژی دورانی.
خودت امتحان کن
(پیشرفته) مراجع و مطالعه بیشتر
- موانع چرخش داخلی در مورد اوراق قرضه منفرد
جان پی لو
پیشرفت در شیمی آلی فیزیکی (ویرایشهای A. Streitwieser و RW Taft).1969، جلد 6.
DOI: 10.1002/9780470171851.ch1
این فصل کتاب مطالعاتی را از منابع بسیاری در مورد موانع چرخش داخلی در مولکولهای کوچک مانند پروپان گردآوری میکند. - حالتهای فرکانس پایین در کریستالهای مولکولی IX پیچ خوردگی های متیل و موانع چرخش داخلی برخی از مولکول های سه بالا
جی آر دوریگ، مجله فیزیک شیمی 53:1، 38-50 1970
DOI: 10.1063/1.1673792
بسیار فنی است، اما یک محاسبه از مانع چرخشی به 2-متیل پروپان در 3.94 کیلو کالری در مول دارد.
